En el ámbito de la biología y la química, es común escuchar los términos catalizador y enzima. Aunque ambos términos se utilizan para describir sustancias que aceleran reacciones químicas, existen diferencias fundamentales entre ellos. Este artículo se adentrará en las características de cada uno, sus funciones, y cómo se relacionan en el contexto de las reacciones químicas. Comprender estas diferencias es esencial para estudiantes y profesionales que trabajan en campos relacionados con la ciencia.
Definición de catalizador
Un catalizador es una sustancia que aumenta la velocidad de una reacción química sin ser consumido en el proceso. Esto significa que, al final de la reacción, el catalizador sigue estando presente y puede ser utilizado nuevamente. Los catalizadores pueden ser de origen orgánico o inorgánico y se encuentran en diversas aplicaciones, desde la industria química hasta la producción de energía. Un ejemplo común de un catalizador es el platino, que se utiliza en convertidores catalíticos de automóviles para reducir las emisiones nocivas.
La función principal de un catalizador es proporcionar un camino alternativo para la reacción, uno que requiere menos energía para que ocurra. Esto se logra al disminuir la energía de activación, que es la cantidad de energía necesaria para iniciar una reacción. Al hacerlo, los catalizadores permiten que las reacciones ocurran más rápidamente y a temperaturas más bajas, lo que es fundamental en muchas aplicaciones industriales.
 Diferencia entre el ADN plasmídico y el ADN cromosómico
Diferencia entre el ADN plasmídico y el ADN cromosómicoDefinición de enzima
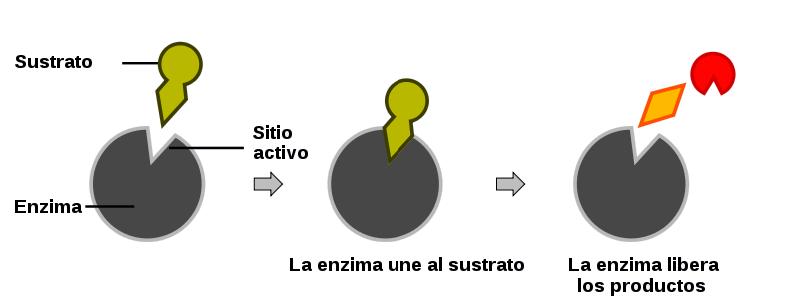
Las enzimas son un tipo específico de catalizador que se encuentra en los organismos vivos. Están compuestas principalmente de proteínas y son esenciales para casi todas las funciones biológicas. Las enzimas catalizan reacciones bioquímicas, facilitando procesos como la digestión, la síntesis de ADN y la producción de energía en las células. A diferencia de los catalizadores inorgánicos, las enzimas son altamente específicas, lo que significa que cada enzima generalmente actúa sobre un solo tipo de sustrato.
Las enzimas funcionan al unirse a sus sustratos en un sitio específico, conocido como el sito activo. Esta unión provoca un cambio en la estructura de la enzima, lo que facilita la transformación del sustrato en producto. Este proceso es conocido como el modelo de llave y cerradura, donde solo la “llave” correcta (el sustrato) puede encajar en la “cerradura” (el sitio activo de la enzima).
Diferencias clave entre catalizadores y enzimas
Existen varias diferencias clave entre catalizadores y enzimas, y es importante comprenderlas para apreciar sus roles en la química y la biología. En primer lugar, la composición es una diferencia significativa. Mientras que los catalizadores pueden ser tanto orgánicos como inorgánicos, las enzimas son casi exclusivamente proteínas. Esto significa que las enzimas tienen estructuras más complejas y específicas que los catalizadores inorgánicos.
 Diferencia entre esporofila y esporangios
Diferencia entre esporofila y esporangiosOtra diferencia importante es la especificidad. Las enzimas son altamente específicas y suelen catalizar solo un tipo de reacción o actuar sobre un solo sustrato. En contraste, muchos catalizadores inorgánicos pueden actuar sobre una variedad de reacciones. Esta especificidad de las enzimas es crucial para la regulación de las reacciones bioquímicas en el cuerpo, asegurando que ocurran de manera controlada y eficiente.
Comparación de características
- Composición: Las enzimas son proteínas; los catalizadores pueden ser orgánicos o inorgánicos.
- Especificidad: Las enzimas son altamente específicas; los catalizadores pueden ser más generales.
- Condiciones de funcionamiento: Las enzimas funcionan en condiciones biológicas; los catalizadores pueden operar en una variedad de condiciones químicas.
- Regulación: Las enzimas pueden ser reguladas por inhibidores y activadores; los catalizadores no suelen estar sujetos a este tipo de regulación.
Ejemplos de catalizadores
Los catalizadores tienen una amplia variedad de aplicaciones en la industria. Un ejemplo clásico es el uso de catalizadores metálicos en la producción de amoníaco a través del proceso Haber. En este proceso, se utilizan catalizadores de hierro para facilitar la reacción entre el nitrógeno y el hidrógeno, lo que resulta en la producción de amoníaco, un compuesto esencial para la fabricación de fertilizantes.
Otro ejemplo notable es el uso de catalizadores en la industria automotriz. Los convertidores catalíticos utilizan metales preciosos como el platino y el paladio para convertir gases nocivos, como el monóxido de carbono y los hidrocarburos, en productos menos dañinos, como el dióxido de carbono y el agua. Esta aplicación es fundamental para reducir la contaminación del aire y mejorar la calidad ambiental.
 Diferencia entre glicación y glicosilación
Diferencia entre glicación y glicosilaciónEjemplos de enzimas
Las enzimas son cruciales en numerosos procesos biológicos. Un ejemplo común es la amilasa, que se encuentra en la saliva y en el páncreas. Esta enzima descompone los almidones en azúcares simples, facilitando la digestión de los carbohidratos. Sin la amilasa, nuestro cuerpo tendría dificultades para absorber energía de los alimentos que consumimos.
Otro ejemplo es la lipasa, que se encarga de descomponer las grasas en ácidos grasos y glicerol. Esta enzima es esencial para la digestión de los lípidos y se produce en el páncreas y el intestino delgado. La lipasa permite que el cuerpo utilice las grasas como fuente de energía, lo que es vital para el funcionamiento adecuado de las células.
Importancia de los catalizadores y enzimas en la industria
La importancia de los catalizadores y enzimas en la industria no puede ser subestimada. En la industria química, los catalizadores son fundamentales para aumentar la eficiencia de las reacciones, lo que se traduce en menores costos de producción y menor impacto ambiental. La capacidad de los catalizadores para acelerar reacciones sin ser consumidos significa que se pueden utilizar de manera continua, lo que mejora la sostenibilidad de los procesos industriales.
En la industria alimentaria, las enzimas son utilizadas para mejorar la calidad de los productos y facilitar la producción. Por ejemplo, se utilizan enzimas en la fabricación de pan para mejorar la textura y el sabor. Asimismo, en la producción de bebidas, como el vino y la cerveza, las enzimas ayudan en la fermentación y en la clarificación del producto final. Sin estas enzimas, muchos de los alimentos que consumimos hoy en día no tendrían las características deseadas.
El papel de los catalizadores y enzimas en la sostenibilidad
En el contexto actual de la sostenibilidad, tanto los catalizadores como las enzimas desempeñan un papel crucial. La búsqueda de procesos más ecológicos ha llevado a un aumento en el uso de catalizadores que operan a temperaturas más bajas y presiones más bajas, reduciendo así el consumo de energía. Por ejemplo, en la producción de biocombustibles, se están utilizando catalizadores que permiten la conversión de biomasa en combustibles de manera más eficiente y menos contaminante.
Por otro lado, las enzimas también están siendo exploradas como una alternativa sostenible en diversos procesos industriales. Las enzimas pueden facilitar reacciones que, de otro modo, requerirían condiciones extremas, lo que reduce la huella de carbono de los procesos industriales. Además, su alta especificidad significa que pueden utilizarse para producir productos de manera más selectiva, minimizando los subproductos y residuos.
Investigación y desarrollo en catalizadores y enzimas
La investigación en el campo de los catalizadores y enzimas es un área activa y en constante evolución. Científicos de todo el mundo están trabajando para descubrir nuevos catalizadores que sean más eficientes y respetuosos con el medio ambiente. En la actualidad, se están desarrollando catalizadores basados en materiales renovables y se están investigando nuevos métodos para sintetizar catalizadores con propiedades mejoradas.
En cuanto a las enzimas, la ingeniería de proteínas es un campo emocionante que busca modificar enzimas existentes para mejorar su rendimiento y estabilidad. Esto puede incluir la alteración de su estructura para que funcionen en condiciones más extremas, como temperaturas más altas o en medios ácidos. La investigación en este ámbito no solo tiene aplicaciones en la industria alimentaria, sino también en la producción de biocombustibles, productos farmacéuticos y otros sectores.
Futuro de los catalizadores y enzimas
El futuro de los catalizadores y enzimas parece prometedor, ya que la necesidad de procesos más eficientes y sostenibles continúa creciendo. A medida que la industria busca reducir su impacto ambiental, el desarrollo de nuevos catalizadores y enzimas será crucial. Los avances en la nanotecnología y la biotecnología están abriendo nuevas posibilidades para la creación de catalizadores y enzimas que sean aún más efectivos y específicos.
Además, el enfoque en la economía circular y la sostenibilidad está impulsando la investigación hacia el uso de catalizadores y enzimas en procesos de reciclaje y reutilización de materiales. Esto podría conducir a una reducción significativa de desechos y un uso más eficiente de los recursos, beneficiando tanto al medio ambiente como a la economía.
aunque los catalizadores y las enzimas comparten la función de acelerar reacciones químicas, sus diferencias en composición, especificidad y aplicación son fundamentales para comprender su papel en la ciencia. Ambos son esenciales en la industria y la biología, y su investigación continúa siendo un área de gran interés. A medida que el mundo avanza hacia un futuro más sostenible, el desarrollo y la aplicación de catalizadores y enzimas serán clave para enfrentar los desafíos ambientales y mejorar la eficiencia de los procesos industriales.