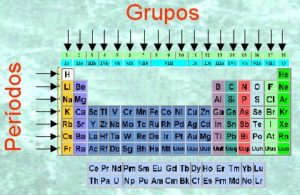
En la tabla periódica, la organización de los elementos químicos se realiza de manera que facilita su estudio y comprensión. Uno de los conceptos fundamentales en este contexto es la diferencia entre períodos y grupos. Estos dos términos son esenciales para entender cómo se comportan los elementos y cómo se relacionan entre sí. Los períodos son las filas horizontales de la tabla periódica, mientras que los grupos son las columnas verticales. A continuación, exploraremos en profundidad qué son los períodos y los grupos, así como sus características y la importancia que tienen en la química.
¿Qué son los períodos?
Los períodos son las filas horizontales de la tabla periódica. Cada período representa un nivel de energía en el que se encuentran los electrones de los átomos de los elementos. A medida que nos movemos de izquierda a derecha a través de un período, los elementos muestran un cambio gradual en sus propiedades. Por ejemplo, el primer período contiene solo dos elementos: el hidrógeno y el helio. Estos elementos son muy diferentes entre sí, lo que resalta la diversidad de propiedades que pueden encontrarse en los diferentes períodos.
Los elementos en un mismo período no tienen características químicas similares, pero sí muestran tendencias en sus propiedades físicas. A medida que avanzamos de izquierda a derecha, la electronegatividad de los elementos generalmente aumenta, mientras que su radio atómico disminuye. Estas tendencias son importantes porque nos ayudan a predecir cómo reaccionarán los elementos en diferentes situaciones químicas.
 Diferencia entre lente cóncava y convexa
Diferencia entre lente cóncava y convexaTendencias en los períodos
- Electronegatividad: Aumenta de izquierda a derecha.
- Radio atómico: Disminuye de izquierda a derecha.
- Potencial de ionización: Aumenta de izquierda a derecha.
- Estado de oxidación: Varía a lo largo del período.
Un aspecto interesante de los períodos es que el número de elementos en cada uno varía. Por ejemplo, el primer período solo contiene dos elementos, mientras que el segundo y el tercer período contienen ocho elementos cada uno. Esta variabilidad en la cantidad de elementos se debe a la forma en que se llenan los niveles de energía en los átomos. En resumen, los períodos son fundamentales para entender la estructura de la tabla periódica y las propiedades de los elementos.
¿Qué son los grupos?
Los grupos, por otro lado, son las columnas verticales de la tabla periódica. Los elementos que se encuentran en un mismo grupo comparten propiedades químicas similares debido a que tienen el mismo número de electrones en su capa más externa, conocida como la capa de valencia. Esta similitud en la configuración electrónica es la razón por la cual los elementos de un mismo grupo tienden a reaccionar de manera similar en reacciones químicas. Por ejemplo, los metales alcalinos, que se encuentran en el grupo 1, son altamente reactivos y tienden a perder un electrón en sus reacciones.
Los grupos se numeran del 1 al 18 en la tabla periódica moderna. Dentro de estos grupos, podemos encontrar familias de elementos que tienen características comunes. Por ejemplo, el grupo 17, conocido como los halógenos, incluye elementos como el flúor, el cloro y el yodo, todos los cuales son altamente reactivos y forman compuestos con metales y no metales. Esta clasificación en grupos facilita la comprensión de las propiedades químicas de los elementos y permite predecir sus comportamientos en diversas reacciones.
 Diferencia entre periostio y endostio
Diferencia entre periostio y endostioCaracterísticas de los grupos
- Similitud química: Los elementos en un mismo grupo tienen propiedades químicas similares.
- Número de electrones de valencia: Comparten el mismo número de electrones en su capa de valencia.
- Reactividad: La reactividad de los elementos puede variar dentro de un grupo.
- Familias de elementos: Los grupos pueden clasificarse en familias como metales, no metales y metales de transición.
La comprensión de los grupos es crucial para los químicos, ya que les permite anticipar cómo interactuarán los elementos entre sí. Por ejemplo, al estudiar el grupo de los metales de transición, los químicos pueden predecir la formación de compuestos complejos y sus propiedades únicas. Así, los grupos son esenciales para el estudio de la química y la predicción de comportamientos en reacciones químicas.
Diferencias clave entre períodos y grupos
Ahora que hemos definido períodos y grupos, es importante destacar las diferencias clave entre ellos. En primer lugar, los períodos son filas horizontales, mientras que los grupos son columnas verticales. Esta simple distinción visual es fundamental para entender la organización de la tabla periódica. Además, los elementos en un mismo período no comparten propiedades químicas similares, mientras que los elementos en un mismo grupo sí lo hacen.
Otra diferencia importante es que los períodos están relacionados con los niveles de energía de los electrones, mientras que los grupos están relacionados con la configuración electrónica de los electrones de valencia. Esto significa que, al estudiar un período, nos enfocamos en cómo varían las propiedades a medida que avanzamos en la tabla, mientras que al estudiar un grupo, nos concentramos en cómo los elementos comparten características químicas debido a su configuración electrónica.
 Diferencia entre perispermo y endospermo
Diferencia entre perispermo y endospermoComparación de características
- Ubicación: Los períodos son horizontales; los grupos son verticales.
- Propiedades: Los elementos en un período no comparten propiedades; los elementos en un grupo sí.
- Niveles de energía: Los períodos están relacionados con niveles de energía; los grupos están relacionados con electrones de valencia.
- Tendencias: Los períodos muestran tendencias en propiedades; los grupos muestran similitudes en reactividad.
Estas diferencias son fundamentales para la química, ya que nos permiten organizar y clasificar los elementos de manera efectiva. Además, esta clasificación ayuda a los científicos a realizar predicciones sobre las propiedades y comportamientos de los elementos, lo que es esencial para la investigación y el desarrollo de nuevos materiales y compuestos.
Importancia de la tabla periódica
La tabla periódica es una herramienta invaluable en la química y otras ciencias. Su organización en períodos y grupos permite a los científicos clasificar los elementos de manera efectiva y estudiar sus propiedades. Además, la tabla periódica proporciona información crucial sobre la reactividad de los elementos, su estado físico a temperatura ambiente y sus propiedades químicas y físicas. Sin esta organización, sería extremadamente difícil entender las relaciones entre los diferentes elementos y cómo interactúan en diversas reacciones.
La tabla periódica también es esencial en la educación. Desde la escuela primaria hasta la universidad, los estudiantes aprenden sobre los elementos y sus propiedades a través de esta herramienta. La comprensión de los períodos y grupos es fundamental para construir una base sólida en química. Sin esta base, los estudiantes pueden encontrar dificultades para comprender conceptos más avanzados en química y ciencias relacionadas.
Aplicaciones de la tabla periódica
- Investigación científica: Utilizada para predecir reacciones y propiedades de nuevos compuestos.
- Industria química: Fundamental para la producción de productos químicos y materiales.
- Educación: Herramienta clave para enseñar conceptos básicos de química.
- Desarrollo de nuevos materiales: Ayuda a identificar combinaciones de elementos para crear nuevos materiales.
La capacidad de predecir el comportamiento de los elementos a partir de su posición en la tabla periódica es una de las razones por las que esta herramienta es tan valiosa. Los científicos pueden, por ejemplo, prever cómo un elemento reaccionará con otro basándose únicamente en su ubicación en la tabla. Esto ha llevado a importantes avances en la ciencia y la tecnología, y ha permitido a los investigadores desarrollar nuevos compuestos y materiales con propiedades específicas.
Ejemplos de períodos y grupos en acción
Para entender mejor la diferencia entre períodos y grupos, es útil ver ejemplos concretos de elementos en la tabla periódica. Tomemos, por ejemplo, el carbono (C), que se encuentra en el período 2 y el grupo 14. El carbono es un elemento fundamental para la vida, ya que forma parte de todas las moléculas orgánicas. Al estar en el período 2, tiene un total de 6 electrones, lo que le permite formar enlaces covalentes con otros elementos, como el hidrógeno y el oxígeno.
En contraste, consideremos el potasio (K), que se encuentra en el grupo 1 y el período 4. El potasio es un metal alcalino altamente reactivo. Debido a que está en el grupo 1, tiene un solo electrón en su capa de valencia, lo que lo hace muy propenso a perder ese electrón y formar compuestos iónicos. Este comportamiento reactivo es característico de todos los elementos en el grupo 1, como el sodio (Na) y el litio (Li).
Comparación de elementos
- Carbono (C): Período 2, Grupo 14, forma enlaces covalentes.
- Potasio (K): Período 4, Grupo 1, altamente reactivo.
- Flúor (F): Período 2, Grupo 17, forma compuestos con metales.
- Hierro (Fe): Período 4, Grupo 8, metal de transición.
Estos ejemplos ilustran cómo la posición de un elemento en la tabla periódica influye en sus propiedades y comportamientos químicos. Los elementos en el mismo grupo comparten características similares, mientras que los elementos en el mismo período muestran una variedad de propiedades a medida que se avanza de izquierda a derecha. Esta estructura organizada permite a los químicos y científicos en general comprender mejor la naturaleza de los elementos y cómo interactúan entre sí.
Conclusiones sobre períodos y grupos
La comprensión de la diferencia entre períodos y grupos es fundamental para cualquier persona interesada en la química y las ciencias relacionadas. Los períodos y grupos no solo organizan los elementos de manera visualmente atractiva, sino que también proporcionan un marco para entender las propiedades y comportamientos de los elementos. Al estudiar la tabla periódica, los científicos pueden hacer predicciones sobre cómo los elementos interactuarán en diferentes condiciones, lo que es esencial para el desarrollo de nuevos materiales y la investigación científica en general.
Al final, la tabla periódica es mucho más que una simple lista de elementos. Es una herramienta poderosa que ha revolucionado nuestra comprensión de la química y nos ha permitido hacer avances significativos en una variedad de campos. La diferencia entre períodos y grupos es solo un aspecto de la rica y compleja historia de la química, pero es un aspecto que todos deberían entender para apreciar completamente la belleza y el orden del mundo químico.