El orden de enlace es una propiedad fundamental en la química que nos ayuda a entender la estabilidad de una molécula. Este concepto se deriva de la teoría de los orbitales moleculares, que describe cómo los electrones se distribuyen en los orbitales de una molécula. Para calcular el orden de enlace a partir del diagrama de orbitales moleculares, es necesario seguir un proceso sistemático que incluye la identificación de los orbitales ocupados y la aplicación de una fórmula sencilla. En este artículo, abordaremos en detalle cómo se realiza este cálculo y la importancia de entender el orden de enlace en la química.
Qué son los orbitales moleculares
Los orbitales moleculares son regiones del espacio donde es probable encontrar electrones en una molécula. A diferencia de los orbitales atómicos, que se encuentran en los átomos individuales, los orbitales moleculares se forman cuando dos o más átomos se unen. Cuando los átomos se acercan, sus orbitales atómicos pueden combinarse para formar nuevos orbitales, que se denominan orbitales moleculares. Existen dos tipos principales de orbitales moleculares: los orbitales enlazantes y los orbitales antienlazantes.
Los orbitales enlazantes son aquellos que favorecen la formación de enlaces entre átomos. Estos orbitales se crean cuando los orbitales atómicos se combinan de tal manera que la probabilidad de encontrar electrones entre los núcleos atómicos aumenta. Por otro lado, los orbitales antienlazantes se forman cuando los orbitales atómicos se combinan de manera que la probabilidad de encontrar electrones entre los núcleos disminuye, lo que debilita el enlace. Entender la diferencia entre estos tipos de orbitales es crucial para calcular el orden de enlace.
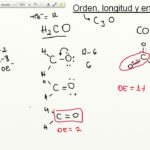 Cómo calcular el orden y la longitud de los enlaces Ciencia
Cómo calcular el orden y la longitud de los enlaces Ciencia¿Qué es el orden de enlace?
El orden de enlace es un número que indica cuántos enlaces existen entre dos átomos en una molécula. Este número se puede calcular utilizando la siguiente fórmula:
- Orden de enlace = (número de electrones en orbitales enlazantes – número de electrones en orbitales antienlazantes) / 2
El resultado de esta fórmula nos proporciona una medida de la estabilidad del enlace. Un orden de enlace de 1 indica un enlace simple, un orden de enlace de 2 indica un enlace doble, y un orden de enlace de 3 indica un enlace triple. Por lo tanto, el orden de enlace no solo nos dice cuántos enlaces hay, sino también la fuerza y la estabilidad de esos enlaces en la molécula.
Cómo construir un diagrama de orbitales moleculares
Para calcular el orden de enlace, primero debemos construir un diagrama de orbitales moleculares. Este diagrama nos ayudará a visualizar cómo se distribuyen los electrones en los diferentes orbitales de la molécula. El primer paso es identificar los átomos que forman la molécula y contar el número total de electrones de valencia. Los electrones de valencia son aquellos que se encuentran en la capa más externa de los átomos y son responsables de la formación de enlaces.
 Cómo calcular el peso molecular de un polímero Ciencia
Cómo calcular el peso molecular de un polímero CienciaUna vez que tengamos el número total de electrones de valencia, debemos distribuir estos electrones en los orbitales moleculares. Comenzamos llenando los orbitales enlazantes más bajos en energía antes de pasar a los orbitales de mayor energía. Es importante seguir el principio de Aufbau, que establece que los electrones ocuparán primero los orbitales de menor energía. Además, debemos tener en cuenta el principio de exclusión de Pauli, que indica que no puede haber dos electrones en un mismo orbital con los mismos números cuánticos.
Ejemplo práctico: Cálculo del orden de enlace
Tomemos como ejemplo la molécula de nitrógeno (N2). El nitrógeno tiene 5 electrones de valencia por átomo, por lo que la molécula de nitrógeno tiene un total de 10 electrones de valencia. Al construir el diagrama de orbitales moleculares para N2, los electrones se distribuyen de la siguiente manera:
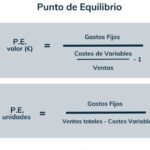 Cómo calcular el punto de equilibrio Negocios
Cómo calcular el punto de equilibrio Negocios- 2 electrones en el orbital sigma (σ) 1s (enlazante)
- 2 electrones en el orbital sigma (σ*) 1s (antienlazante)
- 2 electrones en el orbital sigma (σ) 2s (enlazante)
- 2 electrones en el orbital sigma (σ*) 2s (antienlazante)
- 2 electrones en el orbital sigma (σ) 2p (enlazante)
- 2 electrones en el orbital pi (π) 2p (enlazante)
Con esta distribución, podemos contar los electrones en los orbitales enlazantes y antienlazantes. En N2, tenemos 8 electrones en orbitales enlazantes (2 en σ1s + 2 en σ2s + 2 en σ2p + 2 en π2p) y 2 electrones en orbitales antienlazantes (2 en σ*1s + 2 en σ*2s). Aplicando la fórmula del orden de enlace:
- Orden de enlace = (8 – 2) / 2 = 3
Por lo tanto, el orden de enlace de la molécula de nitrógeno es 3, lo que indica que hay un enlace triple entre los átomos de nitrógeno.
Importancia del orden de enlace
El orden de enlace tiene una gran importancia en la química, ya que nos ayuda a predecir la estabilidad de una molécula. Un mayor orden de enlace generalmente indica una mayor estabilidad y fuerza del enlace. Por ejemplo, las moléculas con enlaces triples, como el nitrógeno, son mucho más estables que las que tienen enlaces simples. Además, el orden de enlace puede influir en las propiedades físicas y químicas de una sustancia, como su punto de ebullición y su reactividad.
Además, el orden de enlace es fundamental para entender la química orgánica e inorgánica. Por ejemplo, en la química orgánica, los enlaces entre carbonos son esenciales para la formación de estructuras complejas. Comprender cómo se forman y rompen estos enlaces es crucial para el diseño de nuevos compuestos y materiales. Asimismo, en la química inorgánica, el orden de enlace puede ayudar a explicar las propiedades de los metales de transición y sus compuestos.
Factores que afectan el orden de enlace
Existen varios factores que pueden influir en el orden de enlace de una molécula. Uno de los factores más importantes es la electronegatividad de los átomos involucrados en el enlace. La electronegatividad es la tendencia de un átomo a atraer electrones hacia sí mismo. Cuando dos átomos con diferentes electronegatividades forman un enlace, puede haber una distribución desigual de electrones, lo que puede afectar la estabilidad del enlace y, por ende, su orden de enlace.
Otro factor que puede influir en el orden de enlace es la hibridación de los orbitales atómicos. La hibridación se refiere a la combinación de orbitales atómicos para formar nuevos orbitales que se utilizan en la formación de enlaces. Por ejemplo, en el caso del etileno (C2H4), los átomos de carbono utilizan orbitales sp2 hibridados para formar enlaces dobles, lo que resulta en un orden de enlace de 1.5. La hibridación, por lo tanto, puede tener un impacto significativo en el orden de enlace de una molécula.
Relación entre el orden de enlace y la energía de enlace
La energía de enlace es otra propiedad relacionada con el orden de enlace. Generalmente, a medida que aumenta el orden de enlace, también aumenta la energía de enlace. Esto se debe a que los enlaces más fuertes requieren más energía para romperse. Por ejemplo, los enlaces simples tienen menor energía de enlace en comparación con los enlaces dobles o triples. La relación entre el orden de enlace y la energía de enlace es crucial para entender cómo se comportan las moléculas en diferentes condiciones.
Además, la energía de enlace es un factor importante en las reacciones químicas. Durante una reacción, los enlaces en los reactivos deben romperse antes de que se formen nuevos enlaces en los productos. La cantidad de energía necesaria para romper los enlaces se relaciona directamente con el orden de enlace. Por lo tanto, comprender el orden de enlace nos ayuda a predecir la energía necesaria para llevar a cabo una reacción química.
Aplicaciones del cálculo del orden de enlace
El cálculo del orden de enlace tiene diversas aplicaciones en la química y la ciencia de materiales. En el ámbito de la química orgánica, se utiliza para diseñar nuevas moléculas y compuestos con propiedades específicas. Por ejemplo, los químicos pueden manipular el orden de enlace en los compuestos orgánicos para desarrollar nuevos fármacos que sean más efectivos o menos tóxicos.
En la química inorgánica, el orden de enlace es fundamental para entender la estructura y la reactividad de los compuestos de metales de transición. Estos compuestos a menudo presentan diferentes órdenes de enlace, lo que influye en sus propiedades magnéticas y catalíticas. Comprender cómo se relaciona el orden de enlace con estas propiedades es crucial para el desarrollo de nuevos materiales y tecnologías.
Limitaciones del modelo de orbitales moleculares
Si bien el modelo de orbitales moleculares es una herramienta poderosa para entender la química de las moléculas, también tiene sus limitaciones. Una de las principales limitaciones es que el modelo no siempre puede explicar adecuadamente el comportamiento de moléculas más complejas. Por ejemplo, en algunos casos, la teoría de orbitales moleculares puede no predecir con precisión la geometría molecular o la energía de los enlaces.
Además, el modelo asume que los electrones se distribuyen de manera uniforme en los orbitales, lo que puede no ser el caso en moléculas con efectos de resonancia o estructuras no tradicionales. En estos casos, es posible que se necesiten enfoques más avanzados, como la teoría del funcional de la densidad (DFT), para obtener una descripción más precisa de la distribución de electrones en una molécula.
Conclusiones sobre el cálculo del orden de enlace
El cálculo del orden de enlace a partir del diagrama de orbitales moleculares es un proceso esencial en la química que nos permite entender la estabilidad y la fuerza de los enlaces en las moléculas. Al seguir un enfoque sistemático para construir el diagrama y aplicar la fórmula del orden de enlace, podemos obtener información valiosa sobre las propiedades de las moléculas. A medida que avanzamos en la química, el conocimiento del orden de enlace se convierte en una herramienta fundamental para el diseño y la manipulación de compuestos químicos en diversas aplicaciones.
