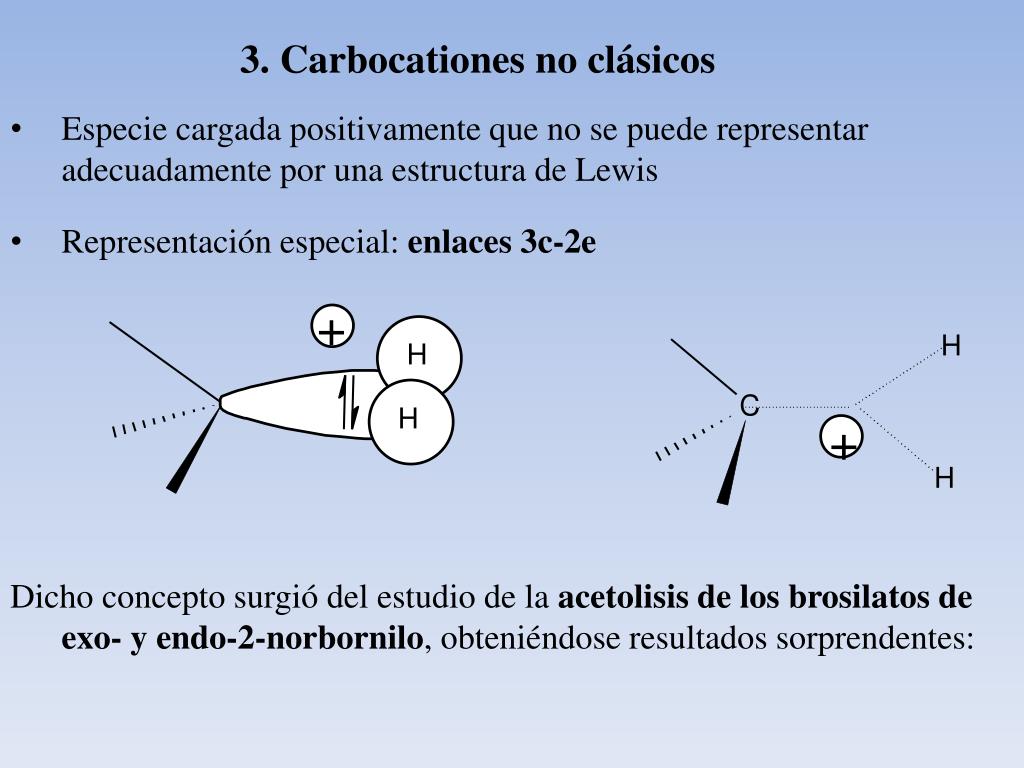
Los carbocationes son especies químicas que contienen un átomo de carbono con una carga positiva. Esta carga positiva se genera porque el carbono tiene solo tres enlaces, lo que significa que le falta un electrón para completar su octeto. Existen dos tipos principales de carbocationes: los carbocationes clásicos y los carbocationes no clásicos. Cada uno de estos tipos presenta características y propiedades únicas que son importantes en la química orgánica. A continuación, exploraremos en detalle las diferencias entre estos dos tipos de carbocationes.
Carbocatión Clásico
Los carbocationes clásicos son aquellos que tienen un carbono central con una carga positiva y están rodeados por otros átomos, generalmente hidrógenos o grupos alquilo. En este tipo de carbocatión, la carga positiva se localiza en un solo átomo de carbono. Esta estructura es bastante sencilla y fácil de entender, ya que la carga positiva se manifiesta claramente en el carbono que carece de un enlace. Por ejemplo, el carbocatión más simple es el ion metilo (CH3+), donde el carbono tiene tres enlaces y una carga positiva.
Una característica importante de los carbocationes clásicos es su estabilidad. La estabilidad de un carbocatión clásico depende de su entorno. Por ejemplo, los carbocationes terciarios son más estables que los secundarios, y estos son más estables que los primarios. Esta estabilidad se debe a la capacidad de los grupos alquilo adyacentes para donar electrones y estabilizar la carga positiva en el carbono. La teoría de la estabilización del carbocatión clásico se basa en el concepto de inducción y resonancia.
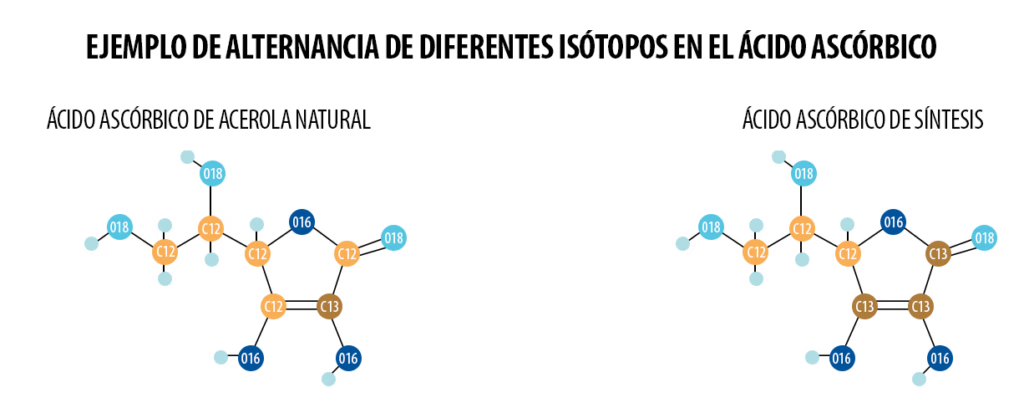 Diferencia entre el ácido ascórbico y el ácido L-ascórbico
Diferencia entre el ácido ascórbico y el ácido L-ascórbicoFactores que Afectan la Estabilidad de los Carbocationes Clásicos
- Inducción Electrónica: Los grupos alquilo que rodean al carbocatión pueden donar electrones a través de enlaces sigma, lo que ayuda a estabilizar la carga positiva.
- Resonancia: En algunos casos, la carga positiva puede ser deslocalizada a través de un sistema de enlaces dobles, lo que también contribuye a la estabilidad.
- Hibridación: Los carbocationes con hibridación sp2 (como los carbocationes terciarios) son más estables que aquellos con hibridación sp3.
Los carbocationes clásicos son esenciales en muchos procesos químicos, como la reacción de sustitución nucleofílica y la eliminación. En estas reacciones, la formación de un carbocatión clásico es un paso intermedio crucial. Por lo tanto, comprender su comportamiento y estabilidad es fundamental para predecir los resultados de diversas reacciones químicas en la química orgánica.
Carbocatión No Clásico
Los carbocationes no clásicos, por otro lado, presentan una estructura más compleja. En lugar de tener una carga positiva localizada en un solo carbono, la carga positiva puede estar deslocalizada a través de un sistema de enlaces. Esto significa que la carga no está confinada a un solo átomo, sino que puede ser compartida entre varios átomos en la molécula. Un ejemplo famoso de un carbocatión no clásico es el ion ciclopropilcarbocatión, donde la carga positiva se distribuye a través de un sistema de anillo.
La deslocalización de la carga positiva en los carbocationes no clásicos proporciona una mayor estabilidad en comparación con los carbocationes clásicos. Esto se debe a que la carga positiva puede ser «distribuida» entre varios átomos, lo que reduce la densidad de carga positiva en un solo punto. Esta estabilidad adicional es especialmente importante en reacciones químicas donde la formación de carbocationes es un paso crítico.
 Diferencia entre genes dominantes y recesivos
Diferencia entre genes dominantes y recesivosEjemplos de Carbocationes No Clásicos
- Ión Ciclopropilcarbocatión: Este carbocatión presenta una carga positiva en un sistema de anillo, lo que permite una mayor deslocalización.
- Ión Norbornilcarbocatión: En este caso, la carga positiva se encuentra en una estructura cíclica que permite la resonancia y la deslocalización.
- Ión Allylcarbocatión: La carga positiva en este carbocatión puede ser deslocalizada a través de enlaces dobles, lo que contribuye a su estabilidad.
La presencia de carbocationes no clásicos en las reacciones químicas puede influir en la velocidad y el resultado de la reacción. Debido a su mayor estabilidad, estos carbocationes pueden ser intermediarios preferidos en ciertas reacciones, lo que lleva a la formación de productos específicos. Por lo tanto, el estudio de los carbocationes no clásicos es fundamental para entender la reactividad en química orgánica.
Diferencias Clave entre Carbocatión Clásico y No Clásico
La diferencia principal entre los carbocationes clásicos y no clásicos radica en la localización de la carga positiva. En los carbocationes clásicos, la carga positiva está restringida a un solo átomo de carbono, mientras que en los carbocationes no clásicos, la carga se deslocaliza a través de varios átomos. Esta diferencia en la distribución de la carga tiene implicaciones significativas en la estabilidad de cada tipo de carbocatión. La estabilidad de los carbocationes clásicos se basa en la inducción y la resonancia, mientras que los carbocationes no clásicos se benefician de la deslocalización de la carga positiva.
 Diferencia entre la inmunidad mediada por anticuerpos y la inmunidad mediada por células
Diferencia entre la inmunidad mediada por anticuerpos y la inmunidad mediada por célulasOtro aspecto a considerar es la reactividad. Los carbocationes clásicos suelen ser más reactivos debido a su menor estabilidad, lo que significa que están más dispuestos a participar en reacciones químicas. Por otro lado, los carbocationes no clásicos, al ser más estables, pueden ser menos reactivos, pero también pueden ser intermediarios en reacciones más complejas donde se requiere una mayor estabilidad. Esta reactividad y estabilidad son factores clave a la hora de prever el comportamiento de las moléculas en reacciones químicas.
Impacto en la Química Orgánica
- Mecanismos de Reacción: La presencia de carbocationes clásicos o no clásicos puede cambiar el mecanismo de una reacción.
- Selección de Productos: Los carbocationes no clásicos pueden llevar a la formación de productos diferentes debido a su estabilidad.
- Estudio de Intermediarios: Comprender estos carbocationes es esencial para el diseño de nuevas reacciones químicas en la investigación orgánica.
La importancia de entender la diferencia entre los carbocationes clásicos y no clásicos se extiende más allá de la química básica. En el desarrollo de nuevos medicamentos y materiales, la comprensión de cómo estos intermediarios químicos afectan la reactividad y la estabilidad puede ser crucial. Por ejemplo, en la síntesis de fármacos, los químicos pueden necesitar predecir cómo se comportarán los carbocationes en condiciones específicas para optimizar la producción de compuestos deseados.
Ejemplos en la Práctica Química
En la práctica química, los carbocationes se forman en diversas reacciones, y entender la diferencia entre los carbocationes clásicos y no clásicos puede ayudar a los químicos a predecir los resultados de estas reacciones. Por ejemplo, en una reacción de adición de electrófilos, un carbocatión clásico puede formarse como intermediario, lo que puede llevar a la formación de productos específicos. Si un carbocatión no clásico está involucrado, la reacción puede seguir un camino diferente debido a la mayor estabilidad del intermediario.
Un ejemplo clásico es la reacción de eliminación de E1, donde se forma un carbocatión como intermediario. En este tipo de reacción, la estabilidad del carbocatión influye en la velocidad de la reacción. Si se forma un carbocatión clásico, la reacción puede ser más rápida debido a la menor estabilidad, mientras que un carbocatión no clásico puede llevar a un producto más estable, pero a una reacción más lenta. Esta diferencia es fundamental para la planificación de síntesis en química orgánica.
Reacciones Comunes que Involucran Carbocationes
- Reacciones de Adición Electrofílica: Los carbocationes son intermediarios comunes en estas reacciones, donde se añade un electrófilo a un doble enlace.
- Reacciones de Eliminación: La formación de carbocationes es un paso clave en reacciones de eliminación, como E1 y E2.
- Reacciones de Sustitución: Los carbocationes pueden ser intermediarios en reacciones de sustitución nucleofílica, como S_N1.
La comprensión de cómo los carbocationes se forman y se comportan en diferentes reacciones es esencial para los químicos que trabajan en la síntesis de compuestos orgánicos. La elección de un enfoque específico en la síntesis puede depender de la naturaleza del carbocatión que se forma y de si es clásico o no clásico. Este conocimiento permite a los químicos manipular las condiciones de reacción para obtener los productos deseados de manera más eficiente.
Conclusiones sobre Carbocationes Clásicos y No Clásicos
los carbocationes clásicos y no clásicos son fundamentales en la química orgánica, cada uno con sus propias características y comportamientos. La diferencia clave entre ellos radica en la localización de la carga positiva y cómo esto afecta su estabilidad y reactividad. A medida que los químicos continúan investigando y desarrollando nuevas reacciones, la comprensión de estos conceptos se vuelve cada vez más importante. Al estudiar los carbocationes, los científicos pueden predecir mejor los resultados de las reacciones y optimizar la síntesis de compuestos útiles.
La química es un campo en constante evolución, y el estudio de los carbocationes es solo una parte de un panorama mucho más amplio. A medida que se desarrollan nuevas técnicas y herramientas, es probable que nuestra comprensión de estos intermediarios químicos se profundice aún más. Esto no solo enriquecerá nuestro conocimiento de la química, sino que también abrirá nuevas puertas para la innovación en la ciencia y la tecnología.