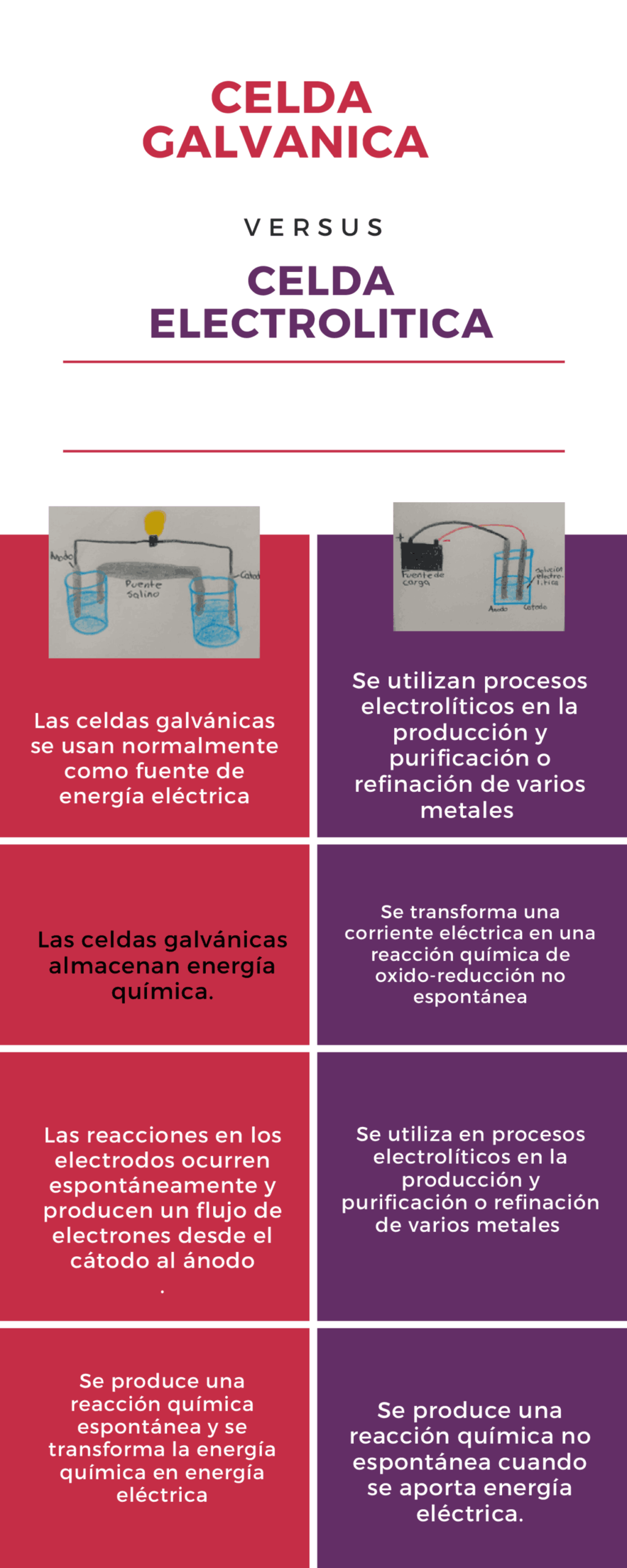
La diferencia entre celda galvánica y electrolítica es un tema fundamental en el estudio de la electroquímica. Ambas celdas son dispositivos que permiten la conversión de energía química en energía eléctrica, pero operan de manera opuesta y tienen diferentes aplicaciones. Las celdas galvánicas, también conocidas como celdas voltaicas, generan electricidad de forma espontánea a partir de reacciones químicas. Por otro lado, las celdas electrolíticas requieren un suministro externo de energía eléctrica para llevar a cabo reacciones químicas no espontáneas. A continuación, se explorarán en detalle las características, aplicaciones y funcionamiento de cada tipo de celda.
Celda Galvánica
Las celdas galvánicas son dispositivos que convierten la energía química en energía eléctrica de manera espontánea. Estas celdas funcionan gracias a una reacción redox, donde ocurre la oxidación en un electrodo y la reducción en otro. La parte de la celda donde ocurre la oxidación se llama ánodo, mientras que la parte donde ocurre la reducción se llama cátodo. El flujo de electrones desde el ánodo al cátodo a través de un circuito externo es lo que genera la corriente eléctrica.
Un ejemplo común de celda galvánica es la batería. Las baterías están diseñadas para almacenar energía química y liberarla en forma de energía eléctrica cuando es necesario. Este proceso ocurre de manera continua mientras haya reactivos disponibles. La reacción que tiene lugar en la celda galvánica es espontánea, lo que significa que no se requiere energía externa para que la reacción ocurra. Esto hace que las celdas galvánicas sean muy útiles en aplicaciones donde se necesita una fuente de energía portátil.
 Diferencia entre cromatina y nucleosoma
Diferencia entre cromatina y nucleosomaCaracterísticas de la Celda Galvánica
- Genera electricidad de manera espontánea.
- Consta de dos electrodos: ánodo y cátodo.
- Requiere un medio conductor (electrolito) para el flujo de iones.
- Utiliza reacciones redox para funcionar.
En una celda galvánica, el electrolito es esencial, ya que permite la movilidad de iones entre los electrodos. Esto es crucial para mantener el equilibrio de carga y facilitar la reacción química. La eficiencia de una celda galvánica puede verse afectada por factores como la concentración de los reactivos y la temperatura. A medida que la reacción avanza, la concentración de los reactivos disminuye, lo que puede afectar la generación de corriente eléctrica.
Celda Electrolítica
Las celdas electrolíticas funcionan de manera opuesta a las galvánicas. En este caso, la energía eléctrica se utiliza para impulsar una reacción química que no sería espontánea. Este tipo de celda se emplea en procesos como la electrólisis, donde se separan los compuestos químicos en sus elementos constitutivos. Por ejemplo, la electrólisis del agua produce hidrógeno y oxígeno a partir de agua utilizando energía eléctrica.
Una celda electrolítica también tiene un ánodo y un cátodo, pero en este caso, el ánodo es el electrodo positivo y el cátodo es el electrodo negativo. Cuando se aplica una corriente eléctrica, los iones positivos se mueven hacia el cátodo, donde ganan electrones (reducción), mientras que los iones negativos se mueven hacia el ánodo, donde pierden electrones (oxidación). Este proceso requiere un suministro constante de energía eléctrica para continuar.
 Diferencia entre la membrana celular y la membrana nuclear
Diferencia entre la membrana celular y la membrana nuclearCaracterísticas de la Celda Electrolítica
- Requiere energía eléctrica externa para funcionar.
- Se utiliza para llevar a cabo reacciones químicas no espontáneas.
- Consta de dos electrodos: ánodo y cátodo.
- Utiliza reacciones redox, pero en sentido opuesto al de las celdas galvánicas.
El uso de celdas electrolíticas se extiende a diversas aplicaciones industriales, como la electrodeposición, donde se recubren objetos metálicos con una capa de metal para mejorar su resistencia a la corrosión. También se utilizan en la producción de productos químicos, como el cloro y el hidróxido de sodio a partir de la electrólisis de la salmuera. Estos procesos son esenciales en la industria química y en la fabricación de productos cotidianos.
Comparación entre Celdas Galvánicas y Electrolíticas
Al comparar las celdas galvánicas y electrolíticas, es importante tener en cuenta varios factores, como su funcionamiento, aplicaciones y eficiencia. Mientras que las celdas galvánicas generan electricidad de forma espontánea, las celdas electrolíticas requieren una fuente de energía externa. Esto significa que las celdas galvánicas son ideales para aplicaciones donde se necesita energía eléctrica de manera continua y portátil, como en dispositivos electrónicos y vehículos eléctricos.
Por otro lado, las celdas electrolíticas son más útiles en procesos industriales donde se requiere la producción de sustancias químicas específicas. Por ejemplo, en la industria del aluminio, se utilizan celdas electrolíticas para extraer aluminio metálico a partir de su mineral, la bauxita. Este proceso es altamente eficiente y permite la producción de grandes cantidades de aluminio a un costo relativamente bajo.
 Diferencia entre mutación germinal y somática
Diferencia entre mutación germinal y somáticaDiferencias Clave
- Las celdas galvánicas generan electricidad; las electrolíticas requieren electricidad.
- Las reacciones en celdas galvánicas son espontáneas; en celdas electrolíticas son no espontáneas.
- Las celdas galvánicas son comunes en baterías; las electrolíticas se usan en procesos industriales.
- Las celdas galvánicas son más simples en su diseño; las electrolíticas requieren un sistema de alimentación de energía.
La eficiencia de ambas celdas también puede variar. En general, las celdas galvánicas tienden a ser más eficientes en la conversión de energía química a eléctrica, mientras que las celdas electrolíticas pueden tener pérdidas significativas de energía en forma de calor durante el proceso de electrólisis. Sin embargo, la elección entre una celda galvánica y una electrolítica dependerá del propósito específico y de las necesidades del proceso en cuestión.
Aplicaciones de las Celdas Galvánicas
Las celdas galvánicas tienen una amplia gama de aplicaciones en la vida cotidiana y en diversas industrias. Una de las aplicaciones más comunes es en las baterías recargables, como las de iones de litio que se utilizan en teléfonos móviles, computadoras portátiles y vehículos eléctricos. Estas baterías son esenciales para el funcionamiento de dispositivos electrónicos, ya que permiten el almacenamiento y la liberación de energía eléctrica de manera eficiente.
Además de las baterías, las celdas galvánicas se utilizan en celdas de combustible, que convierten directamente la energía química del hidrógeno y el oxígeno en electricidad. Estas celdas son prometedoras para el futuro de la energía, ya que producen solo agua como subproducto, lo que las hace más limpias y sostenibles en comparación con los combustibles fósiles. Las celdas de combustible están siendo exploradas como una alternativa viable para el transporte y la generación de energía a gran escala.
Ejemplos de Aplicaciones
- Baterías de iones de litio en dispositivos electrónicos.
- Celdas de combustible para vehículos de hidrógeno.
- Fuentes de energía portátil para dispositivos médicos.
- Fuentes de energía de respaldo en sistemas de energía renovable.
Otras aplicaciones incluyen el uso de celdas galvánicas en sistemas de protección catódica, donde se utilizan para prevenir la corrosión en estructuras metálicas, como tuberías y tanques de almacenamiento. Al aplicar una corriente eléctrica, se impide la corrosión del metal, lo que prolonga la vida útil de las estructuras y reduce costos de mantenimiento. Este tipo de aplicación es crucial en la industria del petróleo y gas, así como en la construcción de infraestructuras.
Aplicaciones de las Celdas Electrolíticas
Las celdas electrolíticas también tienen una variedad de aplicaciones industriales y científicas. Una de las aplicaciones más comunes es en la producción de metales a partir de sus minerales. Por ejemplo, la electrólisis se utiliza para extraer aluminio del mineral de bauxita, lo que es fundamental para la industria del aluminio. Este proceso permite la obtención de metal puro a partir de compuestos químicos complejos.
Además, las celdas electrolíticas son utilizadas en la electrodeposición, un proceso que recubre objetos metálicos con una capa de otro metal. Este proceso se utiliza en la fabricación de componentes electrónicos, joyería y en la industria automotriz para mejorar la resistencia a la corrosión y la apariencia de los productos. La electrodeposición permite un control preciso sobre el grosor y la calidad de la capa depositada.
Ejemplos de Aplicaciones
- Producción de aluminio mediante electrólisis.
- Electrodeposición de metales en componentes electrónicos.
- Fabricación de productos químicos, como el cloro y el hidróxido de sodio.
- Recubrimientos protectores en la industria automotriz.
Otro uso importante de las celdas electrolíticas es en la purificación de metales. Este proceso permite eliminar impurezas de metales como el cobre y el níquel, mejorando su calidad y rendimiento en aplicaciones industriales. La purificación electrolítica es esencial en la producción de metales de alta pureza que se utilizan en la electrónica, la energía y otras industrias avanzadas.
Aspectos Técnicos y Eficiencia
Desde un punto de vista técnico, tanto las celdas galvánicas como las electrolíticas tienen sus ventajas y desventajas en términos de eficiencia. Las celdas galvánicas suelen ser más eficientes en la conversión de energía química en eléctrica, con un rendimiento que puede superar el 90% en condiciones óptimas. Esto las hace ideales para aplicaciones donde la eficiencia energética es crucial, como en baterías y sistemas de energía renovable.
Por otro lado, las celdas electrolíticas suelen tener una eficiencia más baja debido a las pérdidas de energía en forma de calor y otros factores. Sin embargo, la eficiencia de las celdas electrolíticas puede mejorarse mediante el uso de tecnologías avanzadas y la optimización de los parámetros del proceso, como la temperatura y la concentración de electrolitos. Esto es especialmente importante en aplicaciones industriales donde se requiere una producción continua y eficiente.
Factores que Afectan la Eficiencia
- Concentración de reactivos en la celda.
- Temperatura de operación.
- Diseño del electrodo y material utilizado.
- Condiciones del electrolito.
La elección entre una celda galvánica y una electrolítica dependerá en gran medida de la aplicación específica y de los requisitos de eficiencia. En algunos casos, puede ser más beneficioso utilizar una celda galvánica para aplicaciones de energía portátil, mientras que en otros, las celdas electrolíticas son preferibles para la producción de sustancias químicas y metales. La comprensión de estos aspectos técnicos es fundamental para el desarrollo y la mejora de tecnologías basadas en la electroquímica.
Perspectivas Futuras
El futuro de las celdas galvánicas y electrolíticas es prometedor, con avances en tecnología que podrían mejorar su eficiencia y ampliar su rango de aplicaciones. En el caso de las celdas galvánicas, la investigación se centra en el desarrollo de baterías de nueva generación que ofrezcan una mayor capacidad de almacenamiento, tiempos de carga más rápidos y una vida útil más larga. Esto es crucial para el crecimiento de la movilidad eléctrica y la adopción de energías renovables.
Por otro lado, las celdas electrolíticas también están en el centro de la investigación, especialmente en el ámbito de la producción de hidrógeno como fuente de energía limpia. La electrólisis del agua es vista como una solución potencial para la producción de hidrógeno a partir de fuentes renovables, lo que podría ayudar a descarbonizar el sector energético. El desarrollo de celdas electrolíticas más eficientes y sostenibles es un área clave de investigación en el contexto de la transición energética.
Tendencias Emergentes
- Desarrollo de baterías de estado sólido.
- Mejoras en la eficiencia de la electrólisis del agua.
- Investigación en materiales avanzados para electrodos.
- Integración de celdas en sistemas de energía renovable.
Además, se están explorando nuevas tecnologías y materiales que podrían revolucionar tanto las celdas galvánicas como las electrolíticas. La investigación en nanotecnología y materiales avanzados puede conducir a mejoras significativas en la eficiencia y el rendimiento de estas celdas. A medida que la demanda de energía limpia y sostenible continúa creciendo, es probable que la electroquímica juegue un papel cada vez más importante en el futuro energético del mundo.