En la química, es fundamental entender la naturaleza de las sustancias que forman parte de nuestro entorno. Dos categorías importantes de sustancias son los compuestos estequiométricos y los compuestos no estequiométricos. La diferencia entre estos dos tipos de compuestos radica principalmente en su composición y en cómo se forman. A continuación, exploraremos en detalle qué son estos compuestos, sus características y cómo se diferencian entre sí.
¿Qué son los compuestos estequiométricos?
Los compuestos estequiométricos son aquellos que tienen una composición definida y constante. Esto significa que en un compuesto estequiométrico, los elementos que lo componen están presentes en proporciones fijas. Por ejemplo, el agua (H₂O) es un compuesto estequiométrico porque siempre está formada por dos átomos de hidrógeno y uno de oxígeno. Esta proporción no cambia, independientemente de la cantidad de agua que se esté considerando.
Estos compuestos se pueden representar mediante fórmulas químicas, que indican la cantidad de cada tipo de átomo presente. En el caso del agua, la fórmula H₂O muestra que hay dos átomos de hidrógeno por cada átomo de oxígeno. Esta representación es esencial para la comprensión de las reacciones químicas, ya que permite a los científicos y estudiantes predecir cómo reaccionarán diferentes compuestos entre sí.
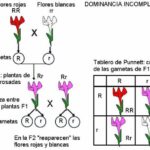 Diferencia entre dominancia completa e incompleta
Diferencia entre dominancia completa e incompletaAdemás, los compuestos estequiométricos suelen ser estables y tienen propiedades físicas y químicas bien definidas. Por ejemplo, la temperatura de ebullición y el punto de fusión del agua son constantes y se conocen con precisión. Esta estabilidad es una de las razones por las que los compuestos estequiométricos son tan importantes en la química y en diversas aplicaciones científicas y tecnológicas.
¿Qué son los compuestos no estequiométricos?
Por otro lado, los compuestos no estequiométricos son aquellos que no tienen una composición fija. Esto significa que la proporción de los elementos que los componen puede variar. Un ejemplo clásico de un compuesto no estequiométrico es el óxido de hierro, que puede presentarse en diferentes proporciones de hierro y oxígeno, como FeO (óxido de hierro(II)) y Fe₂O₃ (óxido de hierro(III)). La variabilidad en la composición es una característica clave de estos compuestos.
Los compuestos no estequiométricos a menudo se forman a través de procesos como la solidificación o la precipitación, donde los elementos se combinan de manera que no se mantiene una proporción constante. Esto puede dar lugar a una serie de compuestos que contienen diferentes cantidades de los mismos elementos, lo que resulta en propiedades físicas y químicas distintas.
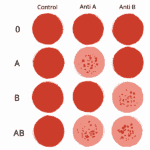 Diferencia entre el grupo sanguíneo Bombay y el grupo sanguíneo O
Diferencia entre el grupo sanguíneo Bombay y el grupo sanguíneo OUna de las características más interesantes de los compuestos no estequiométricos es que a menudo presentan propiedades únicas que no se encuentran en sus compuestos estequiométricos. Por ejemplo, pueden exhibir una mayor conductividad eléctrica o propiedades magnéticas que son útiles en aplicaciones tecnológicas, como en la fabricación de imanes o en dispositivos electrónicos.
Diferencias clave entre compuestos estequiométricos y no estequiométricos
La principal diferencia entre los compuestos estequiométricos y no estequiométricos radica en su composición. Mientras que los compuestos estequiométricos tienen proporciones fijas y definidas de sus elementos, los compuestos no estequiométricos pueden variar en su composición. Esta diferencia tiene importantes implicaciones en la forma en que se comportan estos compuestos en diversas reacciones químicas.
- Composición: Los compuestos estequiométricos tienen una composición constante, mientras que los no estequiométricos tienen proporciones variables.
- Estabilidad: Los compuestos estequiométricos suelen ser más estables y predecibles en sus propiedades, mientras que los no estequiométricos pueden ser más inestables.
- Propiedades físicas y químicas: Los compuestos estequiométricos tienen propiedades bien definidas, mientras que los no estequiométricos pueden exhibir propiedades únicas y variadas.
- Formación: Los compuestos estequiométricos se forman mediante reacciones que resultan en proporciones fijas, mientras que los no estequiométricos pueden formarse en condiciones variables.
Ejemplos de compuestos estequiométricos
Existen muchos ejemplos de compuestos estequiométricos en la naturaleza y en la industria. Algunos de los más comunes incluyen el cloruro de sodio (NaCl), que es la sal de mesa, y el ácido sulfúrico (H₂SO₄). En el cloruro de sodio, cada molécula está compuesta por un átomo de sodio y un átomo de cloro, lo que significa que siempre se presenta en una proporción de 1:1.
 Diferencia entre endoesqueleto y exoesqueleto
Diferencia entre endoesqueleto y exoesqueletoOtro ejemplo es el dióxido de carbono (CO₂), que está formado por un átomo de carbono y dos átomos de oxígeno. Al igual que el agua, su composición es fija y no cambia. Estos compuestos son esenciales en muchos procesos biológicos y químicos, como la fotosíntesis y la respiración celular.
En el ámbito industrial, los compuestos estequiométricos son cruciales para la fabricación de productos químicos. Por ejemplo, el amoníaco (NH₃) se utiliza en la producción de fertilizantes y otros productos químicos, y su fórmula indica que está compuesto por un átomo de nitrógeno y tres de hidrógeno, lo que representa una relación constante en todas las muestras de amoníaco.
Ejemplos de compuestos no estequiométricos
En contraste, los compuestos no estequiométricos son igualmente importantes y se encuentran en diversas aplicaciones. Un ejemplo notable es el óxido de titanio (TiO₂), que puede existir en diferentes formas, como el anatasa y el rutilo, dependiendo de la proporción de titanio y oxígeno en su estructura. Estos diferentes tipos de óxido de titanio tienen propiedades físicas y ópticas distintas, lo que los hace útiles en aplicaciones como pigmentos y en la fabricación de dispositivos electrónicos.
Otro ejemplo es el silicato de sodio, que se utiliza en la fabricación de detergentes y productos de limpieza. Este compuesto puede tener diferentes proporciones de silicio, sodio y oxígeno, lo que le confiere propiedades que varían según su composición. Esta variabilidad permite adaptar los productos a diferentes necesidades y aplicaciones.
Los metales de transición también suelen formar compuestos no estequiométricos. Por ejemplo, el óxido de cobalto (CoO) puede tener una composición variable que afecta sus propiedades magnéticas y eléctricas, lo que lo hace valioso en aplicaciones de almacenamiento de energía y en la fabricación de imanes permanentes.
Implicaciones en la química y la industria
La comprensión de la diferencia entre compuestos estequiométricos y no estequiométricos tiene importantes implicaciones en el campo de la química y la industria. En la investigación, la capacidad de predecir la composición y las propiedades de los compuestos es fundamental para el desarrollo de nuevos materiales y productos químicos. Los compuestos estequiométricos, con sus proporciones fijas, permiten a los científicos realizar cálculos precisos en reacciones químicas.
En la industria, la capacidad de manipular la composición de compuestos no estequiométricos puede conducir a la creación de productos innovadores. Por ejemplo, la fabricación de materiales con propiedades específicas, como la conductividad eléctrica o la resistencia a la corrosión, puede depender de la variabilidad en la composición de los compuestos no estequiométricos. Esto es especialmente relevante en la producción de dispositivos electrónicos y en la investigación de nuevos materiales para aplicaciones avanzadas.
Además, la diferencia en la estabilidad entre estos compuestos también tiene implicaciones prácticas. Los compuestos estequiométricos, al ser más estables, son más fáciles de manejar y almacenar, lo que es crucial en la industria química. Por otro lado, los compuestos no estequiométricos, aunque pueden ser más inestables, ofrecen oportunidades para innovaciones en campos como la nanotecnología y la ciencia de materiales.
La importancia de la estequiometría en la educación química
La enseñanza de la química a menudo se centra en la estequiometría, que es la rama de la química que estudia las relaciones cuantitativas entre los reactivos y productos en una reacción química. Esta área del conocimiento es fundamental para que los estudiantes comprendan cómo se forman los compuestos estequiométricos y cómo se llevan a cabo las reacciones químicas. Aprender sobre la estequiometría permite a los estudiantes realizar cálculos precisos y predecir el resultado de las reacciones químicas.
En el aula, los estudiantes suelen aprender a balancear ecuaciones químicas, lo que es esencial para entender la cantidad de reactivos necesarios y los productos formados. Esta habilidad es particularmente útil al trabajar con compuestos estequiométricos, ya que su composición constante facilita el cálculo de proporciones. Sin embargo, también es importante que los estudiantes comprendan la existencia de compuestos no estequiométricos y cómo su variabilidad puede afectar los resultados de las reacciones químicas.
La enseñanza de la química debe incluir ejemplos prácticos y experimentales que muestren tanto los compuestos estequiométricos como los no estequiométricos. Esto no solo ayuda a los estudiantes a comprender mejor la teoría, sino que también les permite apreciar la diversidad y complejidad de la química en el mundo real. La educación en química, por lo tanto, debe abordar ambas categorías de compuestos para proporcionar una comprensión completa y equilibrada del tema.
Conclusión sobre compuestos estequiométricos y no estequiométricos
la diferencia entre compuestos estequiométricos y no estequiométricos es un tema crucial en el estudio de la química. Mientras que los compuestos estequiométricos tienen una composición fija y constante, los compuestos no estequiométricos presentan variabilidad en su composición. Esta diferencia no solo afecta las propiedades de los compuestos, sino que también tiene importantes implicaciones en la investigación, la industria y la educación química. Comprender estas diferencias es esencial para cualquier persona interesada en la química y sus aplicaciones en el mundo real.
