La electronegatividad y la polaridad son conceptos fundamentales en la química que ayudan a entender cómo se comportan los átomos y las moléculas en diferentes situaciones. Aunque están relacionados, cada uno tiene un significado y un uso específico. En este artículo, exploraremos en profundidad la diferencia entre estos dos términos, cómo se miden, y su importancia en la química y en la vida cotidiana.
¿Qué es la electronegatividad?
La electronegatividad es una propiedad de los átomos que indica su capacidad para atraer electrones en un enlace químico. Esta propiedad fue introducida por el químico Linus Pauling en la década de 1930 y se ha convertido en una herramienta esencial para entender las interacciones entre diferentes elementos. La electronegatividad se mide en una escala que va de 0 a 4, donde los elementos más electronegativos, como el flúor, tienen un valor cercano a 4, y los menos electronegativos, como el cesio, tienen valores cercanos a 0.
La electronegatividad no es una propiedad fija; puede variar dependiendo del entorno químico en el que se encuentre el átomo. Sin embargo, en general, los elementos que se encuentran en la parte superior derecha de la tabla periódica, como el oxígeno y el nitrógeno, tienden a ser más electronegativos que aquellos que están en la parte inferior izquierda, como los metales alcalinos. Esta tendencia se debe a la forma en que los electrones están distribuidos alrededor del núcleo del átomo.
 Diferencia entre FKM y FFKM
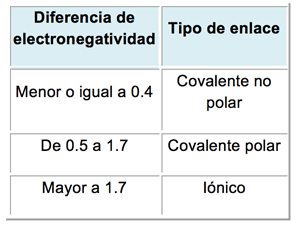
Diferencia entre FKM y FFKMLa electronegatividad es crucial para entender cómo se forman los enlaces químicos. Cuando dos átomos se combinan, la diferencia en su electronegatividad determina el tipo de enlace que se formará. Si la diferencia es grande, se formará un enlace iónico, mientras que si la diferencia es pequeña, se formará un enlace covalente. Esta información es esencial para predecir el comportamiento químico de las moléculas.
¿Qué es la polaridad?
La polaridad se refiere a la distribución de carga eléctrica en una molécula. Una molécula se considera polar si tiene un lado con carga positiva y otro lado con carga negativa, lo que resulta en un dipolo eléctrico. La polaridad es el resultado de la diferencia en electronegatividad entre los átomos que forman la molécula. Cuando hay una diferencia significativa en electronegatividad, los electrones se comparten de manera desigual, creando un dipolo.
Para que una molécula sea polar, no solo debe haber una diferencia en la electronegatividad entre los átomos, sino que también debe tener una geometría que no permita que las cargas se cancelen. Por ejemplo, el agua (H₂O) es una molécula polar porque el oxígeno es más electronegativo que el hidrógeno, lo que crea un dipolo. Además, la forma angular de la molécula evita que las cargas se cancelen, manteniendo la polaridad.
 Diferencia entre oro y pirita
Diferencia entre oro y piritaLa polaridad de una molécula tiene importantes implicaciones en sus propiedades físicas y químicas. Las moléculas polares tienden a ser solubles en disolventes polares, como el agua, mientras que las moléculas no polares son solubles en disolventes no polares, como el aceite. Esta propiedad es fundamental en procesos biológicos y químicos, como la disolución de nutrientes en el cuerpo y la formación de membranas celulares.
Diferencias clave entre electronegatividad y polaridad
Aunque la electronegatividad y la polaridad están interrelacionadas, existen diferencias clave entre ambos conceptos. La electronegatividad se refiere a la capacidad de un átomo para atraer electrones, mientras que la polaridad se refiere a la distribución de carga eléctrica en una molécula. A continuación, se presentan algunas de las diferencias más importantes:
- Definición: La electronegatividad es una propiedad atómica, mientras que la polaridad es una propiedad molecular.
- Medición: La electronegatividad se mide en una escala (como la escala de Pauling), mientras que la polaridad se determina observando la distribución de carga en la molécula.
- Influencia: La electronegatividad afecta la formación de enlaces, mientras que la polaridad afecta las propiedades físicas de las moléculas.
Estas diferencias son fundamentales para comprender cómo interactúan los átomos y las moléculas en diferentes contextos. Por ejemplo, al estudiar la solubilidad de compuestos en agua, es esencial considerar tanto la electronegatividad de los átomos involucrados como la polaridad resultante de la molécula.
 Diferencia entre coliformes fecales y no fecales
Diferencia entre coliformes fecales y no fecalesLa importancia de la electronegatividad en la química
La electronegatividad juega un papel crucial en la química, ya que influye en la formación de enlaces químicos. Cuando dos átomos se combinan, la diferencia en electronegatividad determina el tipo de enlace que se formará. Por ejemplo, si un átomo tiene una electronegatividad mucho mayor que el otro, se formará un enlace iónico, donde uno de los átomos cede electrones y el otro los acepta. En cambio, si la diferencia es pequeña, se formará un enlace covalente, donde los electrones se comparten entre los átomos.
Además, la electronegatividad es esencial para predecir el comportamiento de las reacciones químicas. Al conocer la electronegatividad de los elementos involucrados, los químicos pueden anticipar cómo se comportarán en una reacción, lo que facilita la formulación de nuevos compuestos y materiales. Esto es especialmente importante en la industria farmacéutica, donde se diseñan medicamentos basados en las interacciones químicas entre los compuestos.
Otro aspecto importante es que la electronegatividad influye en las propiedades de los compuestos. Por ejemplo, los compuestos iónicos tienden a tener altos puntos de fusión y ebullición, mientras que los compuestos covalentes pueden tener propiedades muy diferentes dependiendo de su polaridad. Esta variabilidad es fundamental en la creación de nuevos materiales y en la comprensión de cómo se comportan en diferentes condiciones.
La importancia de la polaridad en la química
La polaridad de las moléculas es igualmente crucial en la química, ya que afecta una variedad de propiedades físicas y químicas. Por ejemplo, la solubilidad de un compuesto en un disolvente depende de la polaridad de ambos. Las moléculas polares, como el agua, tienden a disolver otras moléculas polares, mientras que las moléculas no polares se disuelven en disolventes no polares. Esta propiedad es esencial en muchos procesos biológicos, como la absorción de nutrientes y la eliminación de desechos en los organismos.
Además, la polaridad afecta las interacciones intermoleculares. Las moléculas polares pueden formar enlaces de hidrógeno, que son interacciones fuertes entre un átomo de hidrógeno y un átomo electronegativo, como oxígeno o nitrógeno. Estos enlaces son responsables de muchas propiedades del agua, como su alto calor específico y su capacidad para disolver una amplia gama de compuestos. Sin estas propiedades, la vida tal como la conocemos sería imposible.
La polaridad también juega un papel en la química orgánica, donde la disposición de los grupos funcionales en una molécula puede afectar su reactividad y propiedades. Por ejemplo, las moléculas que contienen grupos funcionales polares tienden a ser más reactivas en ciertas condiciones que aquellas que son completamente no polares. Esto permite a los químicos diseñar reacciones específicas y desarrollar nuevos compuestos con propiedades deseadas.
Ejemplos de electronegatividad y polaridad en la vida cotidiana
La electronegatividad y la polaridad están presentes en muchos aspectos de nuestra vida cotidiana. Un ejemplo común es el agua, que es una molécula polar. El oxígeno tiene una electronegatividad mayor que la del hidrógeno, lo que crea un dipolo en la molécula. Esta polaridad es la razón por la cual el agua es un excelente disolvente para muchas sustancias, permitiendo que los nutrientes se disuelvan y se transporten en organismos vivos.
Otro ejemplo es el comportamiento de los aceites y el agua. Los aceites son generalmente no polares, lo que significa que no se mezclan con el agua, que es polar. Esta propiedad es fundamental en la cocina y en la industria, donde se utilizan diferentes tipos de disolventes para separar o combinar sustancias. Por ejemplo, al preparar una vinagreta, el aceite y el vinagre no se mezclan debido a sus diferencias en polaridad, lo que resulta en una emulsión inestable.
Además, los productos de limpieza suelen estar formulados para aprovechar la polaridad de las moléculas. Muchos detergentes tienen una parte polar y otra no polar, lo que les permite interactuar tanto con el agua como con las grasas y aceites. Esto hace que los detergentes sean efectivos para eliminar manchas y suciedad de diversas superficies.
Medición de la electronegatividad
La electronegatividad se mide utilizando varias escalas, siendo la más conocida la escala de Pauling. Esta escala asigna un valor numérico a cada elemento, lo que permite comparar su capacidad para atraer electrones. Por ejemplo, el flúor tiene un valor de 4.0 en la escala de Pauling, lo que lo convierte en el elemento más electronegativo. En contraste, el cesio tiene un valor de 0.7, lo que indica que es menos electronegativo.
Otra escala utilizada es la escala de Mulliken, que calcula la electronegatividad promediando las energías de ionización y las afinidades electrónicas de un elemento. Esta escala es útil para elementos que no se pueden comparar fácilmente con la escala de Pauling. Sin embargo, la escala de Pauling sigue siendo la más comúnmente utilizada en la enseñanza y en la investigación.
Además, la electronegatividad puede influir en la reactividad de los elementos. Por ejemplo, los metales alcalinos, que tienen baja electronegatividad, son muy reactivos y tienden a perder electrones fácilmente, formando cationes. En contraste, los no metales, que tienen alta electronegatividad, son más propensos a ganar electrones y formar aniones. Esta diferencia en comportamiento es fundamental para entender la química de los compuestos y las reacciones.
Medición de la polaridad
La polaridad de una molécula se puede determinar observando la geometría molecular y la electronegatividad de los átomos que la componen. Para medir la polaridad, se pueden usar diferentes métodos, como la espectroscopía o la cromatografía, que ayudan a analizar cómo se comporta una molécula en diferentes condiciones. Sin embargo, la forma más común de evaluar la polaridad es a través de la distribución de cargas en la molécula.
Una molécula es polar si tiene un dipolo eléctrico, lo que significa que hay una separación de cargas en su estructura. Para determinar si una molécula es polar, se puede observar la diferencia en electronegatividad entre los átomos que la componen. Si la diferencia es significativa y la geometría de la molécula no permite que las cargas se cancelen, entonces la molécula es polar.
Además, algunas herramientas computacionales pueden ayudar a predecir la polaridad de las moléculas mediante simulaciones y cálculos teóricos. Estas herramientas son útiles en la investigación química, ya que permiten a los científicos modelar interacciones moleculares y predecir el comportamiento de nuevos compuestos antes de sintetizarlos en el laboratorio.
Relación entre electronegatividad y polaridad
La relación entre electronegatividad y polaridad es fundamental para comprender la química. La diferencia en electronegatividad entre los átomos de una molécula es lo que crea la polaridad. Si dos átomos tienen electronegatividades muy diferentes, la molécula resultante será polar. Por ejemplo, en el caso del agua, el oxígeno es más electronegativo que el hidrógeno, lo que resulta en una distribución desigual de carga y, por lo tanto, en una molécula polar.
Además, la polaridad puede influir en las propiedades de una sustancia. Las moléculas polares tienden a tener puntos de ebullición y fusión más altos que las no polares debido a las interacciones intermoleculares, como los enlaces de hidrógeno. Esta relación es esencial para entender cómo las diferentes sustancias se comportan en diferentes condiciones y en diversas aplicaciones, desde la biología hasta la ingeniería química.
En resumen, la electronegatividad y la polaridad son conceptos interrelacionados que son fundamentales para la comprensión de la química. La electronegatividad determina cómo los átomos interactúan entre sí, mientras que la polaridad resulta de esas interacciones y afecta las propiedades físicas y químicas de las moléculas. Ambos conceptos son esenciales para los químicos y tienen un impacto significativo en muchos aspectos de la vida cotidiana.