La diferencia entre electrones de valencia y electrones libres es un concepto fundamental en la química y la física, especialmente en el estudio de la estructura atómica y la conductividad eléctrica de los materiales. Los electrones son partículas subatómicas que tienen una carga negativa y se encuentran en la corteza de los átomos. Sin embargo, no todos los electrones son iguales ni cumplen las mismas funciones dentro de un átomo o un material. Los electrones de valencia son aquellos que se encuentran en la capa más externa de un átomo y son los responsables de la formación de enlaces químicos. Por otro lado, los electrones libres son aquellos que no están ligados a un átomo en particular y pueden moverse libremente a través de un material, lo que les permite conducir electricidad.
¿Qué son los electrones de valencia?
Los electrones de valencia son aquellos que se encuentran en la capa externa de un átomo, conocida como la capa de valencia. Esta capa es crucial porque determina cómo un átomo interactúa con otros átomos. En la mayoría de los casos, los electrones de valencia son los que participan en la formación de enlaces químicos, ya sea mediante la transferencia de electrones, como en los enlaces iónicos, o mediante el compartimiento de electrones, como en los enlaces covalentes. La cantidad de electrones de valencia que tiene un átomo depende de su posición en la tabla periódica. Por ejemplo, los elementos del grupo 1 tienen un solo electrón de valencia, mientras que los del grupo 18 tienen ocho, lo que los hace muy estables y menos reactivos.
La configuración de los electrones de valencia es fundamental para entender la reactividad química de los elementos. Por ejemplo, los metales tienden a perder electrones de valencia para formar iones positivos, mientras que los no metales suelen ganar electrones para formar iones negativos. Esta diferencia en el comportamiento de los electrones de valencia es lo que permite la formación de compuestos y moléculas, y es esencial para la química orgánica e inorgánica. Además, la capacidad de un átomo para atraer electrones de otros átomos se mide por su electronegatividad, un concepto que está directamente relacionado con la disposición de los electrones de valencia.
 Diferencia entre flácido y plasmolizado
Diferencia entre flácido y plasmolizadoCaracterísticas de los electrones de valencia
- Ubicación: Se encuentran en la capa más externa del átomo.
- Participación en enlaces: Son los responsables de la formación de enlaces químicos.
- Reactividad: Su número y configuración determinan la reactividad del elemento.
- Estabilidad: Los átomos tienden a ser más estables cuando tienen una capa de valencia llena.
¿Qué son los electrones libres?
Los electrones libres son aquellos electrones que no están asociados a un átomo específico y que pueden moverse libremente a través de un material. Estos electrones son particularmente importantes en el estudio de los conductores eléctricos y los semiconductores. En los metales, por ejemplo, los electrones de valencia tienden a desprenderse de sus átomos, lo que permite que se conviertan en electrones libres. Esta propiedad es lo que hace que los metales sean buenos conductores de electricidad, ya que los electrones libres pueden moverse rápidamente bajo la influencia de un campo eléctrico.
La presencia de electrones libres en un material también afecta su conductividad térmica y su capacidad para absorber y emitir luz. En los semiconductores, la cantidad de electrones libres puede ser controlada mediante la adición de impurezas, un proceso conocido como doping. Este control de la densidad de electrones libres es fundamental para el funcionamiento de dispositivos electrónicos como transistores y diodos. En resumen, los electrones libres son esenciales para la electricidad y la electrónica moderna, y su comportamiento es un área de estudio clave en la física y la ingeniería.
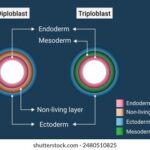 Diferencia entre diploblástico y triploblástico
Diferencia entre diploblástico y triploblásticoCaracterísticas de los electrones libres
- Movilidad: Pueden moverse libremente a través de un material.
- Conductividad: Son responsables de la conductividad eléctrica en los metales.
- Interacción: No están ligados a átomos específicos, lo que les permite interactuar con campos eléctricos.
- Importancia en semiconductores: Su densidad puede ser modificada para controlar las propiedades eléctricas de los materiales.
Comparación entre electrones de valencia y electrones libres
Para entender la diferencia entre electrones de valencia y electrones libres, es útil compararlos en varios aspectos clave. En primer lugar, la ubicación de estos electrones es diferente. Los electrones de valencia se encuentran en la capa más externa de un átomo y son responsables de las interacciones químicas, mientras que los electrones libres están disponibles para moverse a través de un material, lo que les permite conducir electricidad. Esta diferencia en ubicación también implica diferencias en sus funciones: los electrones de valencia participan en la formación de enlaces químicos, mientras que los electrones libres son cruciales para la conductividad eléctrica.
Otra diferencia importante es su comportamiento en respuesta a campos eléctricos. Los electrones de valencia están más restringidos y no pueden moverse libremente, ya que están ligados a sus átomos. En cambio, los electrones libres pueden moverse rápidamente en respuesta a un campo eléctrico, lo que les permite transportar corriente eléctrica. Esto es lo que hace que los materiales conductores, como el cobre y el aluminio, sean tan útiles en aplicaciones eléctricas. Además, los electrones libres son esenciales en la tecnología moderna, como en la fabricación de circuitos y dispositivos electrónicos.
Diferencias clave
- Ubicación: Los electrones de valencia están en la capa externa del átomo; los electrones libres se mueven libremente en un material.
- Función: Los electrones de valencia forman enlaces químicos; los electrones libres conducen electricidad.
- Movilidad: Los electrones de valencia están restringidos; los electrones libres son móviles y responden a campos eléctricos.
- Importancia: Los electrones de valencia son clave para la reactividad química; los electrones libres son esenciales para la conductividad eléctrica.
Ejemplos de electrones de valencia y electrones libres
Un buen ejemplo de electrones de valencia se puede observar en el elemento oxígeno, que tiene seis electrones de valencia. Estos electrones son los responsables de la formación de enlaces con otros átomos, como en la molécula de agua (H₂O), donde el oxígeno se une a dos átomos de hidrógeno mediante enlaces covalentes. La capacidad del oxígeno para atraer electrones también lo convierte en un agente oxidante potente, lo que significa que puede facilitar reacciones químicas en las que se transfieren electrones. Este comportamiento es crucial en muchos procesos biológicos y químicos, como la respiración celular y la fotosíntesis.
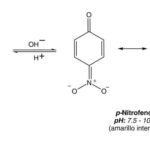 Diferencia entre orto nitrofenol y para nitrofenol
Diferencia entre orto nitrofenol y para nitrofenolEn contraste, un ejemplo de electrones libres se encuentra en los metales como el cobre. En el cobre, los electrones de valencia se separan de sus átomos y se convierten en electrones libres, lo que permite que el cobre conduzca electricidad de manera eficiente. Esta propiedad hace que el cobre sea uno de los materiales más utilizados en la fabricación de cables eléctricos. Además, los electrones libres en el cobre también contribuyen a su capacidad para conducir calor, lo que lo convierte en un excelente material para utensilios de cocina y radiadores.
Ejemplos específicos
- Oxígeno: Tiene seis electrones de valencia que forman enlaces en compuestos como el agua.
- Cobre: Sus electrones de valencia se convierten en electrones libres, permitiendo la conducción eléctrica.
- Carbono: Tiene cuatro electrones de valencia, lo que le permite formar una variedad de compuestos orgánicos.
- Silicio: En semiconductores, sus electrones de valencia pueden ser manipulados para crear electrones libres mediante doping.
Importancia de la comprensión de electrones de valencia y electrones libres
Entender la diferencia entre electrones de valencia y electrones libres es fundamental para diversas disciplinas científicas y tecnológicas. En química, este conocimiento permite a los científicos predecir cómo diferentes elementos interactuarán entre sí. Por ejemplo, al conocer cuántos electrones de valencia tiene un elemento, se puede anticipar su comportamiento en reacciones químicas y la formación de compuestos. Esta información es crucial para el desarrollo de nuevos materiales, fármacos y tecnologías energéticas, entre otros campos.
En el ámbito de la física y la ingeniería, la comprensión de los electrones libres es esencial para el diseño de dispositivos eléctricos y electrónicos. La capacidad de un material para conducir electricidad depende de la cantidad de electrones libres que contiene. Esto es especialmente importante en la fabricación de componentes electrónicos, como transistores y circuitos integrados, que son la base de la tecnología moderna. Sin una comprensión clara de cómo funcionan los electrones de valencia y libres, sería difícil avanzar en estos campos y desarrollar nuevas tecnologías que mejoren nuestras vidas.
Áreas de aplicación
- Química: Predicción de reacciones y desarrollo de nuevos compuestos.
- Física: Estudio de la conductividad y propiedades eléctricas de materiales.
- Ingeniería eléctrica: Diseño de circuitos y dispositivos electrónicos.
- Biología: Comprensión de procesos bioquímicos y reacciones celulares.
Conclusiones sobre electrones de valencia y electrones libres
En resumen, los electrones de valencia y los electrones libres son dos tipos de electrones que desempeñan roles muy diferentes en la química y la física. Mientras que los electrones de valencia son responsables de la formación de enlaces químicos y determinan la reactividad de los elementos, los electrones libres son esenciales para la conducción eléctrica y térmica en materiales. La comprensión de estas diferencias es vital para el avance de la ciencia y la tecnología, y permite a los investigadores y profesionales en estos campos desarrollar nuevas soluciones y productos que impactan nuestras vidas cotidianas.
La interacción entre electrones de valencia y electrones libres también es un área de estudio fascinante que sigue siendo explorada por científicos e ingenieros. La investigación en este campo puede llevar a la creación de nuevos materiales con propiedades eléctricas y térmicas mejoradas, así como a la optimización de procesos químicos y biológicos. En un mundo donde la tecnología y la ciencia continúan avanzando a pasos agigantados, el conocimiento sobre electrones de valencia y electrones libres se vuelve cada vez más relevante y esencial para el futuro.
