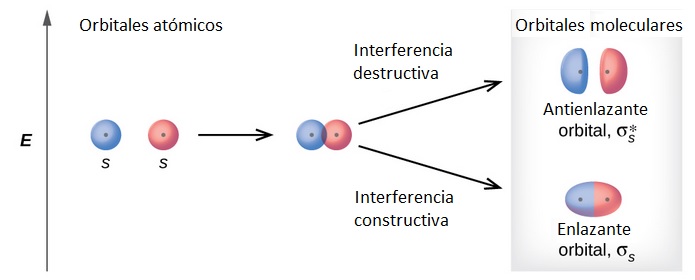
En la química, el concepto de enlaces químicos es fundamental para entender cómo se forman las moléculas. Dentro de este contexto, los electrones enlazantes y los electrones antienlazantes juegan un papel crucial en la formación de enlaces entre átomos. Los electrones enlazantes son aquellos que contribuyen a la estabilidad de un enlace, mientras que los electrones antienlazantes tienden a debilitarlo. Comprender la diferencia entre estos dos tipos de electrones es esencial para estudiar la estructura y propiedades de las moléculas.
¿Qué son los electrones enlazantes?
Los electrones enlazantes son aquellos que se encuentran en orbitales moleculares que favorecen la formación de enlaces entre átomos. Estos electrones se ocupan de tal manera que contribuyen a la estabilidad de la molécula. Por ejemplo, en una molécula diatómica como el hidrógeno (H2), los dos electrones que comparten los dos átomos de hidrógeno están en un orbital molecular enlazante, lo que resulta en una unión fuerte y estable. Este tipo de enlace se caracteriza por la disminución de la energía del sistema, lo que lo hace favorable desde el punto de vista energético.
La presencia de electrones enlazantes en un sistema molecular es fundamental para determinar la geometría y la reactividad de las moléculas. Por ejemplo, en moléculas más complejas, como el agua (H2O), los electrones enlazantes influyen en el ángulo de enlace y, por lo tanto, en la forma de la molécula. En general, cuanto mayor sea el número de electrones enlazantes, más fuerte será el enlace y más estable será la molécula resultante.
 Diferencia entre flagelos y pili
Diferencia entre flagelos y piliCaracterísticas de los electrones enlazantes
- Estabilidad: Contribuyen a la estabilidad de la molécula.
- Baja energía: Se encuentran en orbitales de menor energía.
- Forma de enlace: Definen la geometría y el ángulo de enlace de la molécula.
- Interacción: Interactúan de manera constructiva con los núcleos atómicos.
Además, los electrones enlazantes se distribuyen en orbitales moleculares de forma que maximicen la atracción entre los núcleos de los átomos involucrados. Esto significa que su ubicación y energía son críticas para la formación de enlaces covalentes y la creación de moléculas. En este sentido, los electrones enlazantes se pueden visualizar como aquellos que «unen» los átomos, creando una fuerza que mantiene la estructura molecular intacta.
¿Qué son los electrones antienlazantes?
Por otro lado, los electrones antienlazantes son aquellos que se encuentran en orbitales moleculares que no favorecen la formación de enlaces entre átomos. Estos electrones tienen un efecto opuesto al de los electrones enlazantes, ya que tienden a debilitar el enlace molecular. En términos energéticos, los electrones antienlazantes se encuentran en orbitales de mayor energía y, por lo tanto, su ocupación resulta en un aumento de la energía total del sistema, lo que hace que el enlace sea menos estable.
 Diferencia entre ortocinesis y klinocinesis
Diferencia entre ortocinesis y klinocinesisUn ejemplo clásico de electrones antienlazantes se puede observar en el oxígeno (O2). En esta molécula, hay electrones ocupando tanto orbitales enlazantes como antienlazantes. Aunque el oxígeno tiene un enlace doble, la presencia de electrones en orbitales antienlazantes afecta la estabilidad del enlace. De hecho, si los electrones antienlazantes fueran los únicos presentes, el oxígeno no podría existir como una molécula diatómica estable.
Características de los electrones antienlazantes
- Inestabilidad: Contribuyen a la inestabilidad de la molécula.
- Alta energía: Se encuentran en orbitales de mayor energía.
- Debilitamiento del enlace: Aumentan la energía total del sistema.
- Interacción: Interactúan de manera destructiva con los núcleos atómicos.
Los electrones antienlazantes son un factor determinante en la reactividad de las moléculas. En muchas reacciones químicas, los electrones antienlazantes pueden ser un objetivo para las interacciones con otras moléculas o átomos, ya que su presencia indica que el enlace es más débil y, por lo tanto, más susceptible a romperse. Esta propiedad es crucial en el contexto de la química orgánica y la biología, donde la ruptura de enlaces es un paso esencial en muchas reacciones bioquímicas.
Diferencias clave entre electrones enlazantes y antienlazantes
Las diferencias entre los electrones enlazantes y antienlazantes son fundamentales para comprender la estabilidad y la reactividad de las moléculas. En primer lugar, los electrones enlazantes tienden a reducir la energía total del sistema, mientras que los electrones antienlazantes aumentan esa energía. Esta diferencia en energía es crucial para determinar la viabilidad de una molécula. En segundo lugar, los electrones enlazantes contribuyen a la formación de enlaces estables, mientras que los electrones antienlazantes tienden a debilitar esos enlaces, lo que puede llevar a la ruptura de la molécula bajo ciertas condiciones.
 Diferencia entre el esqueleto masculino y femenino
Diferencia entre el esqueleto masculino y femeninoAdemás, los electrones enlazantes y antienlazantes tienen efectos diferentes en la geometría molecular. Los electrones enlazantes influyen en la forma y el ángulo de los enlaces, mientras que los electrones antienlazantes pueden distorsionar estas características, lo que afecta la reactividad y las propiedades físicas de la molécula. En resumen, la interacción entre estos dos tipos de electrones es lo que determina la estructura y la estabilidad de las moléculas en la química.
Comparación visual de electrones enlazantes y antienlazantes
- Electrones Enlazantes:
- Orbitales de menor energía.
- Contribuyen a la estabilidad del enlace.
- Se encuentran en orbitales moleculares enlazantes.
- Electrones Antienlazantes:
- Orbitales de mayor energía.
- Contribuyen a la inestabilidad del enlace.
- Se encuentran en orbitales moleculares antienlazantes.
Ejemplos de electrones enlazantes y antienlazantes en moléculas
Un buen ejemplo de electrones enlazantes se puede observar en la molécula de metano (CH4). En esta molécula, el carbono forma enlaces con cuatro átomos de hidrógeno mediante la compartición de electrones. Los electrones que se encuentran en los orbitales moleculares que unen el carbono y los hidrógenos son considerados electrones enlazantes. Estos electrones contribuyen a la estabilidad de la molécula, permitiendo que el metano sea un gas estable y común en la naturaleza.
Por otro lado, un ejemplo de electrones antienlazantes se puede encontrar en el dióxido de carbono (CO2). En esta molécula, el carbono forma enlaces dobles con dos átomos de oxígeno. Sin embargo, en el proceso de formación de estos enlaces, también se generan orbitales antienlazantes. Aunque el CO2 es una molécula estable, la presencia de electrones en orbitales antienlazantes significa que, bajo ciertas condiciones, el enlace puede debilitarse, lo que puede llevar a reacciones químicas en las que el CO2 se convierte en otros compuestos.
Importancia de los electrones en la química orgánica
- Reacciones químicas: La presencia de electrones enlazantes y antienlazantes es crucial para entender cómo ocurren las reacciones.
- Estabilidad molecular: Los electrones determinan la estabilidad de las moléculas orgánicas.
- Diseño de fármacos: En la química farmacéutica, se utilizan estos conceptos para diseñar moléculas efectivas.
La comprensión de los electrones enlazantes y antienlazantes no solo es fundamental en la química teórica, sino que también tiene aplicaciones prácticas en campos como la química orgánica, la bioquímica y la medicina. Por ejemplo, en el diseño de nuevos fármacos, los químicos deben considerar cómo los electrones en las moléculas interaccionarán con los objetivos biológicos, lo que requiere un entendimiento profundo de la naturaleza de estos electrones y su impacto en la estabilidad y reactividad de las moléculas.
Teoría de orbitales moleculares
La teoría de orbitales moleculares (TOM) es un modelo que ayuda a explicar cómo se forman los enlaces en las moléculas a través de la combinación de orbitales atómicos. Esta teoría es fundamental para entender la diferencia entre electrones enlazantes y antienlazantes. Según la TOM, cuando los orbitales atómicos de dos átomos se combinan, se forman nuevos orbitales moleculares que pueden ser clasificados como enlazantes o antienlazantes. Los orbitales enlazantes son aquellos que resultan de la superposición constructiva de los orbitales atómicos, mientras que los orbitales antienlazantes resultan de la superposición destructiva.
Un aspecto importante de la TOM es que los electrones ocupan primero los orbitales enlazantes antes de llenar los orbitales antienlazantes. Esto significa que, en una molécula, siempre habrá una tendencia a formar enlaces estables a través de la ocupación de los orbitales de menor energía. La teoría también explica cómo la energía de los electrones en los orbitales antienlazantes contribuye a la inestabilidad del sistema, lo que puede llevar a la ruptura de enlaces bajo ciertas condiciones.
Aplicaciones de la teoría de orbitales moleculares
- Predicción de propiedades: La TOM permite predecir propiedades físicas y químicas de las moléculas.
- Estudio de reacciones: Ayuda a entender cómo y por qué ocurren ciertas reacciones químicas.
- Desarrollo de nuevos materiales: Se utiliza en el diseño de materiales con propiedades específicas.
La TOM tiene un impacto significativo en diversas áreas de la ciencia, incluyendo la química de materiales, la nanotecnología y la biología molecular. Al comprender cómo se comportan los electrones en diferentes tipos de moléculas, los científicos pueden diseñar nuevos materiales con propiedades específicas, desarrollar fármacos más efectivos y explorar nuevas reacciones químicas. Por lo tanto, la teoría de orbitales moleculares es una herramienta esencial en el arsenal de cualquier químico moderno.
Interacciones entre electrones enlazantes y antienlazantes
Las interacciones entre electrones enlazantes y antienlazantes son cruciales para determinar la estabilidad de una molécula. En un sistema molecular, la presencia de ambos tipos de electrones puede influir en cómo se comporta la molécula en diversas condiciones. Por ejemplo, en un entorno donde se aplican altas temperaturas o presiones, los electrones antienlazantes pueden jugar un papel más prominente, debilitando los enlaces y haciendo que la molécula sea más susceptible a la ruptura.
Además, las interacciones entre electrones enlazantes y antienlazantes pueden ser responsables de fenómenos como la resonancia. En sistemas donde existen múltiples estructuras de Lewis, los electrones pueden distribuirse de manera que minimicen la energía total del sistema, lo que lleva a una estabilización adicional. Este fenómeno es común en compuestos aromáticos, donde los electrones se delocalizan a través de la estructura, contribuyendo tanto a la estabilidad como a la reactividad del compuesto.
Ejemplos de interacciones en compuestos químicos
- Compuestos aromáticos: La resonancia y la delocalización de electrones estabilizan las moléculas.
- Reacciones redox: La transferencia de electrones enlazantes y antienlazantes es crucial en estas reacciones.
- Química de coordinación: Los electrones antienlazantes pueden influir en la formación de complejos metálicos.
Las interacciones entre electrones enlazantes y antienlazantes también son importantes en el contexto de la química inorgánica. Por ejemplo, en los complejos de coordinación, la disposición de los electrones puede influir en la forma en que los metales se enlazan con los ligandos. La comprensión de estas interacciones es esencial para el diseño de nuevos compuestos con propiedades específicas, lo que tiene aplicaciones en áreas como la catálisis y el desarrollo de nuevos materiales.
Conclusiones sobre la importancia de los electrones en la química
En resumen, los electrones enlazantes y antienlazantes son conceptos fundamentales en la química que afectan la estabilidad, reactividad y propiedades de las moléculas. A través de la teoría de orbitales moleculares, podemos comprender cómo estos electrones interactúan y contribuyen a la formación de enlaces químicos. Esta comprensión no solo es esencial para la química teórica, sino que también tiene aplicaciones prácticas en campos como la química orgánica, la bioquímica y el diseño de nuevos materiales. La diferencia entre electrones enlazantes y antienlazantes es un aspecto clave en la química que permite a los científicos explorar y manipular el mundo a nivel molecular.