Los enlaces químicos son fundamentales para entender cómo se forman las sustancias y cómo interactúan entre sí. Dentro de los tipos de enlaces químicos, dos de los más importantes son los enlaces covalentes y los enlaces iónicos. Estos dos tipos de enlaces tienen características distintas que determinan las propiedades de las sustancias que los forman. En este artículo, exploraremos en profundidad las diferencias entre estos dos tipos de enlaces, así como sus propiedades, ejemplos y su importancia en la química.
Enlaces Covalentes
Los enlaces covalentes se forman cuando dos átomos comparten uno o más pares de electrones. Este tipo de enlace suele ocurrir entre átomos no metálicos, que tienen electronegatividades similares. La compartición de electrones permite que cada átomo alcance una configuración electrónica más estable, similar a la de los gases nobles. La fuerza del enlace covalente depende de la cantidad de electrones compartidos; por ejemplo, un enlace simple implica el compartimiento de un par de electrones, mientras que un enlace doble implica dos pares.
Una de las características más interesantes de los enlaces covalentes es que pueden ser polares o no polares. En un enlace covalente no polar, los electrones se comparten de manera equitativa entre los átomos, mientras que en un enlace polar, uno de los átomos atrae los electrones con más fuerza, creando una distribución desigual de carga. Esto puede dar lugar a propiedades únicas en las moléculas, como la solubilidad en agua o en aceites.
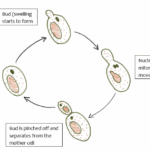 ¿Cómo se reproduce la levadura?
¿Cómo se reproduce la levadura?Características de los Enlaces Covalentes
- Fuerza del enlace: Los enlaces covalentes son generalmente más fuertes que los enlaces iónicos.
- Direccionalidad: Los enlaces covalentes tienen una orientación específica, lo que influye en la forma de la molécula.
- Formación de moléculas: Los enlaces covalentes permiten la formación de moléculas complejas y grandes.
Un ejemplo clásico de un enlace covalente es el agua (H₂O). En esta molécula, cada átomo de hidrógeno comparte un par de electrones con el átomo de oxígeno. Esta compartición de electrones permite que el oxígeno complete su capa de valencia, mientras que los hidrógenos también logran una configuración más estable. Debido a la polaridad del enlace, el agua tiene propiedades únicas, como su capacidad para disolver muchas sustancias, lo que la convierte en un solvente universal.
Enlaces Iónicos
Los enlaces iónicos, en contraste, se forman cuando uno o más electrones son transferidos de un átomo a otro. Este tipo de enlace generalmente ocurre entre átomos con electronegatividades muy diferentes, como un metal y un no metal. Cuando un átomo pierde electrones, se convierte en un ion positivo (cation), mientras que el átomo que gana electrones se convierte en un ion negativo (anión). La atracción electrostática entre estos iones de carga opuesta es lo que mantiene unido al compuesto iónico.
Los compuestos iónicos tienden a formar estructuras cristalinas, donde los iones se organizan en un patrón regular y repetitivo. Esta disposición contribuye a las propiedades características de los compuestos iónicos, como su alta punto de fusión y punto de ebullición. A menudo, estos compuestos son solubles en agua y conducen la electricidad en estado líquido o disueltos, pero son malos conductores en estado sólido debido a la rigidez de su estructura cristalina.
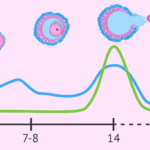 Diferencia entre FSH y LH
Diferencia entre FSH y LHCaracterísticas de los Enlaces Iónicos
- Transferencia de electrones: Los electrones se transfieren de un átomo a otro, formando iones.
- Conductividad: Los compuestos iónicos conducen electricidad en estado líquido o disuelto.
- Solubilidad: Muchos compuestos iónicos son solubles en agua.
Un ejemplo típico de un enlace iónico es el cloruro de sodio (NaCl), más conocido como sal de mesa. En este compuesto, el sodio pierde un electrón para convertirse en un ion positivo, mientras que el cloro gana ese electrón para convertirse en un ion negativo. La atracción entre estos dos iones de carga opuesta forma un enlace iónico, resultando en una estructura cristalina que es altamente soluble en agua.
Diferencias Clave entre Enlaces Covalentes e Iónicos
Existen varias diferencias clave entre los enlaces covalentes e iónicos que son importantes para entender cómo se comportan las sustancias en diferentes condiciones. Una de las diferencias más notables es la forma en que se forman los enlaces. Mientras que los enlaces covalentes se forman a través del compartimiento de electrones, los enlaces iónicos se forman mediante la transferencia de electrones. Esta diferencia en el mecanismo de formación influye en las propiedades físicas y químicas de los compuestos resultantes.
Otra diferencia significativa radica en la fuerza de los enlaces. Generalmente, los enlaces covalentes son más fuertes que los enlaces iónicos, lo que significa que se requiere más energía para romper un enlace covalente. Esto se traduce en compuestos covalentes que tienden a tener puntos de fusión y ebullición más altos que los compuestos iónicos, aunque existen excepciones. Por ejemplo, el agua, que tiene enlaces covalentes, tiene un punto de ebullición relativamente alto en comparación con otros compuestos covalentes simples.
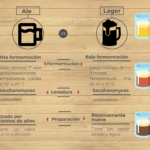 Diferencia entre la fermentación alta y la fermentación baja
Diferencia entre la fermentación alta y la fermentación bajaOtras Diferencias Importantes
- Estado físico: Los compuestos iónicos suelen ser sólidos a temperatura ambiente, mientras que los covalentes pueden ser gases, líquidos o sólidos.
- Solubilidad: Los compuestos iónicos son generalmente solubles en agua, mientras que muchos compuestos covalentes no lo son.
- Conductividad eléctrica: Los compuestos iónicos conducen electricidad en solución, mientras que los compuestos covalentes no lo hacen.
Además, la forma en que se organizan las moléculas también difiere entre estos dos tipos de enlaces. Los compuestos covalentes pueden formar estructuras tridimensionales complejas, mientras que los compuestos iónicos tienden a formar una red cristalina regular. Esta estructura cristalina en los compuestos iónicos es responsable de su dureza y alta temperatura de fusión, características que son muy diferentes en los compuestos covalentes.
Ejemplos de Enlaces Covalentes e Iónicos
Para entender mejor las diferencias entre los enlaces covalentes e iónicos, es útil examinar algunos ejemplos comunes de cada tipo de enlace. En el caso de los enlaces covalentes, el dióxido de carbono (CO₂) es un buen ejemplo. En esta molécula, el carbono forma enlaces covalentes dobles con dos átomos de oxígeno. Estos enlaces son muy estables y dan como resultado una molécula que es lineal en su forma, lo que es crucial para su comportamiento en reacciones químicas.
Por otro lado, el óxido de magnesio (MgO) es un ejemplo típico de un enlace iónico. En este compuesto, el magnesio pierde dos electrones para formar un catión, mientras que el oxígeno gana esos electrones para formar un anión. La atracción electrostática entre estos iones da lugar a un sólido cristalino que es altamente soluble en agua y conduce la electricidad cuando se disuelve.
Más Ejemplos de Enlaces Covalentes
- Metano (CH₄): El carbono forma cuatro enlaces covalentes simples con cuatro átomos de hidrógeno.
- Etano (C₂H₆): Dos átomos de carbono están unidos por un enlace covalente simple, y cada uno se une a hidrógenos.
- Ácido clorhídrico (HCl): El hidrógeno y el cloro comparten un par de electrones.
Más Ejemplos de Enlaces Iónicos
- Fluoruro de sodio (NaF): El sodio transfiere un electrón al flúor, formando un enlace iónico.
- Carbonato de calcio (CaCO₃): Contiene enlaces iónicos entre el calcio y el ion carbonato.
- Cloruro de potasio (KCl): Similar al NaCl, con transferencia de electrones entre potasio y cloro.
Importancia de los Enlaces Covalentes e Iónicos en la Química
La comprensión de los enlaces covalentes e iónicos es crucial en muchos campos de la química y la biología. Los enlaces covalentes son fundamentales en la formación de moléculas biológicas como proteínas, ácidos nucleicos y carbohidratos. Estas moléculas son esenciales para la vida y su estructura se basa en enlaces covalentes que determinan su funcionalidad y propiedades. Por ejemplo, la estructura de la ADN se basa en enlaces covalentes que mantienen unidas las bases nitrogenadas y los azúcares.
Por otro lado, los enlaces iónicos son igualmente importantes en la formación de sales y minerales. Estos compuestos iónicos son esenciales en la naturaleza y en procesos biológicos, como la transmisión de impulsos nerviosos en los organismos. Los iones de sodio y potasio, que forman enlaces iónicos en compuestos como el NaCl y el KCl, son vitales para la función celular y la homeostasis en los seres vivos.
Aplicaciones Prácticas
- Medicina: La comprensión de los enlaces iónicos es fundamental para el desarrollo de medicamentos.
- Industria: Los compuestos covalentes se utilizan en la fabricación de plásticos y otros materiales.
- Alimentos: La sal (NaCl) es un ejemplo de un compuesto iónico utilizado en la preservación de alimentos.
Además, la química de los enlaces covalentes e iónicos tiene aplicaciones en la tecnología. Por ejemplo, los semiconductores, que son fundamentales en la electrónica, a menudo involucran compuestos covalentes. Por otro lado, la química de materiales y la ciencia de los polímeros también se basa en la comprensión de estos enlaces, ya que determinan las propiedades mecánicas y térmicas de los materiales.
la diferencia entre enlaces covalentes e iónicos radica en cómo se forman y las propiedades que resultan de cada tipo de enlace. Los enlaces covalentes se forman mediante el compartimiento de electrones y son típicos en moléculas orgánicas, mientras que los enlaces iónicos se forman por la transferencia de electrones y son comunes en compuestos inorgánicos. Ambos tipos de enlaces son esenciales para la química y tienen un impacto significativo en la biología, la medicina y la tecnología.
