La entalpía y la energía interna son conceptos fundamentales en la termodinámica, una rama de la física que estudia las relaciones entre el calor y otras formas de energía. Estos términos son cruciales para entender cómo funcionan los sistemas físicos y químicos, así como para predecir el comportamiento de las sustancias en diferentes condiciones. Aunque a menudo se utilizan de manera intercambiable, hay diferencias clave entre ambos conceptos que son importantes de comprender. En este artículo, exploraremos en profundidad estas diferencias y cómo se relacionan entre sí.
Definición de energía interna
La energía interna de un sistema se refiere a la energía total contenida en él. Esta energía incluye todas las formas de energía que poseen las partículas que componen el sistema, como la energía cinética debida al movimiento de las moléculas y la energía potencial asociada a las interacciones entre ellas. La energía interna es una propiedad del sistema y depende de su temperatura, volumen y cantidad de sustancia. Es importante destacar que la energía interna no se puede medir directamente, sino que se infiere a partir de cambios en el sistema.
En un sistema cerrado, la energía interna puede cambiar debido a la transferencia de calor o trabajo. Cuando se suministra calor al sistema, la energía interna aumenta, mientras que si se extrae calor, la energía interna disminuye. Por otro lado, cuando se realiza trabajo sobre el sistema, también se incrementa la energía interna, y viceversa. Por lo tanto, la energía interna es una medida de la energía almacenada en un sistema y su variación puede influir en las reacciones químicas y los cambios de fase.
 Diferencia entre caimán y aligátor
Diferencia entre caimán y aligátorDefinición de entalpía
La entalpía es una medida de la cantidad total de energía de un sistema, que incluye tanto la energía interna como la energía asociada a la presión y el volumen del sistema. Se define como la suma de la energía interna y el producto de la presión y el volumen del sistema: H = U + PV, donde H es la entalpía, U es la energía interna, P es la presión y V es el volumen. La entalpía es especialmente útil en procesos que ocurren a presión constante, como reacciones químicas en condiciones atmosféricas.
La entalpía se utiliza comúnmente en la química y la ingeniería para calcular la cantidad de calor involucrado en reacciones químicas y cambios de estado. Cuando se habla de cambios en la entalpía, se refiere a la variación de esta propiedad durante un proceso específico. La variación de entalpía se puede medir y se representa comúnmente como ΔH. Si ΔH es positivo, significa que el sistema ha absorbido calor (reacción endotérmica), mientras que si es negativo, indica que se ha liberado calor (reacción exotérmica).
Diferencias clave entre entalpía y energía interna
Una de las principales diferencias entre entalpía y energía interna radica en su definición y en lo que representan. Mientras que la energía interna se centra únicamente en la energía almacenada en el sistema, la entalpía considera también la energía relacionada con la presión y el volumen. Esto significa que la entalpía es más adecuada para describir procesos que involucran cambios de estado a presión constante, mientras que la energía interna es más relevante en procesos donde el volumen y la presión pueden variar.
 Diferencia entre IgG e IgM contra CMV
Diferencia entre IgG e IgM contra CMVAdemás, la energía interna es una propiedad extensiva, lo que significa que depende de la cantidad de sustancia presente en el sistema. Por otro lado, la entalpía también es extensiva, pero su cálculo incluye factores adicionales como la presión y el volumen. Esto puede llevar a confusiones, especialmente en reacciones químicas, donde es esencial identificar qué propiedad se está utilizando para evaluar el cambio energético del sistema.
Relación entre entalpía y energía interna
A pesar de las diferencias, la entalpía y la energía interna están íntimamente relacionadas. La entalpía se puede considerar como una extensión de la energía interna que incluye el trabajo realizado por el sistema debido a su volumen y presión. En condiciones de presión constante, los cambios en la entalpía pueden ser directamente relacionados con los cambios en la energía interna. Esto se debe a que, en un proceso a presión constante, la cantidad de calor intercambiado es igual a la variación de entalpía.
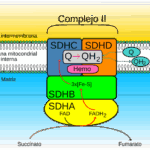 Diferencia entre la fumarato reductasa y la succinato deshidrogenasa
Diferencia entre la fumarato reductasa y la succinato deshidrogenasaPara ilustrar esta relación, se puede considerar una reacción química que ocurre a presión constante. La cantidad de calor absorbido o liberado durante la reacción se puede calcular utilizando la variación de entalpía. Sin embargo, si se desea conocer la energía interna del sistema, se debe tener en cuenta el trabajo realizado por el sistema durante el proceso. Esto demuestra cómo la entalpía y la energía interna interactúan y se complementan entre sí en el estudio de sistemas termodinámicos.
Aplicaciones prácticas de la entalpía y energía interna
En la práctica, tanto la entalpía como la energía interna tienen numerosas aplicaciones en diversas áreas de la ciencia y la ingeniería. En la química, por ejemplo, la entalpía se utiliza para calcular el calor de reacción en procesos químicos. Esto es fundamental para diseñar reactores químicos y optimizar las condiciones de reacción. Conocer la variación de entalpía permite a los químicos predecir si una reacción será espontánea y cuánto calor se liberará o absorberá durante el proceso.
En ingeniería, la entalpía es crucial para el diseño de sistemas de energía, como calderas y turbinas. Los ingenieros utilizan la entalpía para calcular la eficiencia de estos sistemas y optimizar su rendimiento. Por otro lado, la energía interna también es importante en la termodinámica de los gases, donde se utiliza para entender el comportamiento de los gases ideales y reales. Conocer la energía interna de un gas permite predecir cómo cambiará su temperatura y presión bajo diferentes condiciones.
Ejemplos de cálculos de entalpía y energía interna
Para comprender mejor la diferencia entre entalpía y energía interna, consideremos un ejemplo práctico. Imaginemos una reacción química que ocurre a presión constante, como la combustión del metano (CH₄) en presencia de oxígeno (O₂). Durante esta reacción, se liberan productos como dióxido de carbono (CO₂) y agua (H₂O). La variación de entalpía de esta reacción se puede calcular utilizando tablas de entalpía estándar, lo que permite conocer cuánta energía se libera al ambiente.
Supongamos que la variación de entalpía para esta reacción es -890 kJ/mol. Esto indica que se liberan 890 kJ de energía por cada mol de metano quemado. Para calcular la energía interna, tendríamos que considerar el trabajo realizado por los gases durante la expansión y otros factores relacionados con la presión y el volumen. En este caso, aunque la entalpía nos da una idea clara del calor liberado, la energía interna nos proporciona información adicional sobre el sistema durante la reacción.
Medición de la entalpía y energía interna
La medición de la entalpía y la energía interna se lleva a cabo utilizando diferentes técnicas y herramientas. En el caso de la entalpía, los calorímetros son instrumentos comunes que permiten medir el calor absorbido o liberado en una reacción química. Un calorímetro de bomba, por ejemplo, se utiliza para determinar la entalpía de combustión de una sustancia al medir el aumento de temperatura del agua que rodea el calorímetro. Esta variación de temperatura se traduce en un cambio de entalpía que puede ser calculado.
Por otro lado, la energía interna se puede inferir a partir de mediciones de temperatura, volumen y presión de un sistema. En sistemas ideales, se pueden utilizar ecuaciones de estado, como la ecuación de estado de los gases ideales, para calcular la energía interna. Sin embargo, en sistemas reales, donde las interacciones entre moléculas juegan un papel importante, se requiere un análisis más complejo que puede incluir simulaciones y modelos termodinámicos.
Impacto de la temperatura en entalpía y energía interna
La temperatura es un factor crítico que influye tanto en la entalpía como en la energía interna de un sistema. A medida que la temperatura de un sistema aumenta, la energía cinética promedio de las partículas también aumenta, lo que se traduce en un incremento de la energía interna. Este aumento de energía interna, a su vez, puede afectar la entalpía, especialmente en procesos que involucran cambios de fase, como la fusión o la vaporización.
Por ejemplo, al calentar agua, su energía interna aumenta debido al incremento de la energía cinética de las moléculas. Si el agua se calienta hasta alcanzar su punto de ebullición, comenzará a cambiar de estado de líquido a vapor. Durante este proceso, la entalpía del sistema aumentará considerablemente, ya que se requiere calor adicional para superar las fuerzas intermoleculares que mantienen unidas a las moléculas de agua. Este fenómeno resalta la interrelación entre temperatura, entalpía y energía interna en los cambios de estado.
Consideraciones en procesos químicos
En el contexto de los procesos químicos, es esencial entender cómo la entalpía y la energía interna se ven afectadas por las condiciones del sistema. Por ejemplo, en una reacción química que ocurre a temperatura y presión constantes, la variación de entalpía se convierte en una herramienta útil para evaluar la viabilidad de la reacción. Sin embargo, en reacciones que involucran cambios de volumen significativos, como la expansión de gases, la energía interna puede proporcionar información adicional sobre el trabajo realizado por el sistema.
Además, la comprensión de la entalpía y la energía interna es fundamental para el diseño de procesos industriales. Por ejemplo, en la producción de productos químicos, es crucial conocer la cantidad de calor que se liberará o absorberá durante las reacciones para optimizar las condiciones de operación y mejorar la eficiencia energética. Esto puede ayudar a reducir costos y minimizar el impacto ambiental de los procesos químicos.
Enfoques teóricos en entalpía y energía interna
Desde un punto de vista teórico, la entalpía y la energía interna se pueden analizar utilizando principios de la termodinámica. La primera ley de la termodinámica, que establece que la energía no se crea ni se destruye, solo se transforma, es fundamental para comprender cómo se relacionan estas dos propiedades. Esta ley implica que cualquier cambio en la energía interna de un sistema debe ser igual al calor transferido hacia el sistema menos el trabajo realizado por el sistema.
En este sentido, se pueden establecer ecuaciones que relacionen la variación de energía interna y entalpía en diferentes condiciones. Por ejemplo, para un sistema cerrado a presión constante, la variación de entalpía se puede expresar como ΔH = ΔU + PΔV, donde ΔH es el cambio en la entalpía, ΔU es el cambio en la energía interna y PΔV representa el trabajo realizado por el sistema debido a la expansión o contracción. Esta relación es fundamental para el análisis de procesos termodinámicos y para la comprensión de la energía en sistemas químicos y físicos.
Ejemplos de reacciones endotérmicas y exotérmicas
Las reacciones endotérmicas y exotérmicas son ejemplos claros de cómo la entalpía y la energía interna se manifiestan en los procesos químicos. En una reacción endotérmica, como la disolución de cloruro de amonio (NH₄Cl) en agua, se absorbe calor del entorno, lo que resulta en un aumento de la entalpía del sistema. Esto implica que la energía interna del sistema también aumenta debido a la energía absorbida, lo que provoca una disminución de la temperatura del entorno.
Por otro lado, en una reacción exotérmica, como la combustión de la gasolina, se libera calor al entorno, lo que resulta en una disminución de la entalpía del sistema. En este caso, la energía interna del sistema disminuye porque se está realizando trabajo en el entorno al liberar energía en forma de calor. Estos ejemplos resaltan cómo las reacciones químicas pueden influir en la entalpía y la energía interna, y cómo estas propiedades son esenciales para comprender el comportamiento de los sistemas químicos.
La importancia de la entalpía en la industria
En la industria, la entalpía es un concepto clave en el diseño y optimización de procesos. Por ejemplo, en la industria petroquímica, el conocimiento de las variaciones de entalpía en las reacciones de craqueo de hidrocarburos es esencial para maximizar la producción de productos deseados, como gasolina y diésel. Al comprender cómo la entalpía afecta el equilibrio de las reacciones, los ingenieros pueden ajustar las condiciones de operación para mejorar la eficiencia y reducir costos.
Asimismo, en la industria alimentaria, la entalpía juega un papel importante en procesos como la pasteurización y la deshidratación. Conocer la cantidad de calor que se debe transferir durante estos procesos permite a los ingenieros diseñar equipos adecuados y optimizar el consumo energético. Esto no solo mejora la eficiencia de los procesos, sino que también contribuye a la sostenibilidad y reducción del impacto ambiental de la industria.
Implicaciones medioambientales de la entalpía y energía interna
Las consideraciones sobre entalpía y energía interna también tienen implicaciones importantes para el medio ambiente. Por ejemplo, en el contexto del cambio climático, es fundamental comprender cómo las reacciones químicas que involucran la combustión de combustibles fósiles liberan grandes cantidades de energía en forma de calor. Esta liberación de energía, que se traduce en un aumento de la entalpía del sistema, contribuye al calentamiento global y a otros problemas ambientales.
Además, la eficiencia energética de los procesos industriales y la gestión adecuada de la energía interna de los sistemas pueden ayudar a mitigar el impacto ambiental. Al optimizar los procesos para reducir el consumo de energía y minimizar la liberación de calor no deseado, las industrias pueden contribuir a un futuro más sostenible. Esto resalta la importancia de la comprensión de la entalpía y la energía interna en el desarrollo de tecnologías más limpias y eficientes.
Investigación y desarrollo en termodinámica
La investigación en el campo de la termodinámica continúa siendo un área activa de estudio, con un enfoque en la mejora de los modelos que describen la entalpía y la energía interna en sistemas complejos. Los científicos buscan comprender mejor cómo se comportan las sustancias a diferentes temperaturas y presiones, así como las interacciones entre moléculas. Esto puede llevar al desarrollo de nuevos materiales y procesos que sean más eficientes y sostenibles.
Por ejemplo, la investigación en materiales de cambio de fase, que pueden absorber y liberar calor de manera eficiente, se basa en un entendimiento profundo de la entalpía y la energía interna. Estos materiales tienen aplicaciones potenciales en la gestión térmica de edificios, sistemas de almacenamiento de energía y refrigeración. Al avanzar en nuestra comprensión de estos conceptos, los científicos pueden contribuir al desarrollo de tecnologías que aborden desafíos energéticos y medioambientales.
Conclusiones sobre la entalpía y energía interna
La comprensión de la entalpía y la energía interna es esencial para la ciencia y la ingeniería. Estos conceptos no solo son fundamentales para el estudio de la termodinámica, sino que también tienen aplicaciones prácticas en diversas industrias. Desde la química hasta la ingeniería, la capacidad de medir y comprender estas propiedades permite a los profesionales optimizar procesos, mejorar la eficiencia energética y reducir el impacto ambiental. A medida que continuamos explorando estos conceptos, es probable que surjan nuevas oportunidades y desafíos en el camino hacia un futuro más sostenible.
