La entropía y la entalpía son conceptos fundamentales en la termodinámica, una rama de la física que estudia las relaciones entre el calor, el trabajo y la energía. Aunque estos dos términos pueden sonar similares y a menudo se mencionan juntos, representan propiedades muy diferentes de los sistemas termodinámicos. La entropía se relaciona con el desorden y la dirección de los procesos espontáneos, mientras que la entalpía se refiere a la energía total de un sistema a presión constante. Comprender estas diferencias es crucial para cualquier estudiante o profesional que trabaje en campos como la química, la física o la ingeniería.
Definición de Entropía
La entropía es una medida del desorden o la aleatoriedad en un sistema. Se puede entender como una forma de cuantificar la cantidad de energía en un sistema que no está disponible para realizar trabajo. En términos más técnicos, la entropía se relaciona con la cantidad de microestados que corresponden a un macroestado dado. Un macroestado es la descripción general de un sistema, mientras que los microestados son las diferentes maneras en que se puede organizar la energía y la materia dentro de ese sistema.
La entropía se mide en unidades de joules por kelvin (J/K) y es una función de estado, lo que significa que su valor depende solo del estado actual del sistema y no de cómo se llegó a ese estado. En un proceso espontáneo, la entropía de un sistema tiende a aumentar, lo que se conoce como la segunda ley de la termodinámica. Esto implica que los sistemas tienden a evolucionar hacia estados de mayor desorden y menor energía útil.
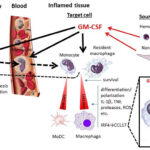 Diferencia entre G-CSF y GM-CSF
Diferencia entre G-CSF y GM-CSFImportancia de la Entropía
- Ayuda a entender la dirección de los procesos espontáneos.
- Es fundamental en la teoría del calor y la energía.
- Se utiliza en el cálculo de la eficiencia de máquinas térmicas.
- Proporciona una base para la comprensión de la química y la biología.
La entropía también juega un papel crucial en la comprensión de fenómenos naturales, como la formación de estructuras complejas en la biología y la evolución de los sistemas físicos. Por ejemplo, en un ecosistema, la energía del sol se convierte en biomasa a través de la fotosíntesis, pero la entropía total del sistema sigue aumentando debido a la energía que se disipa en forma de calor. Esto demuestra que aunque la vida puede parecer ordenada, en un contexto más amplio, la entropía sigue aumentando.
Definición de Entalpía
La entalpía es una medida de la energía total de un sistema, que incluye tanto la energía interna como el trabajo realizado por el sistema sobre su entorno a presión constante. Se define como la suma de la energía interna (U) del sistema más el producto de la presión (P) y el volumen (V) del sistema: H = U + PV. La entalpía se mide en joules (J) y es particularmente útil en procesos químicos y físicos que ocurren a presión constante, como reacciones químicas en un recipiente abierto.
La entalpía se utiliza para calcular el calor absorbido o liberado en reacciones químicas. Por ejemplo, en una reacción exotérmica, la entalpía del sistema disminuye porque se libera calor al entorno. Por otro lado, en una reacción endotérmica, la entalpía aumenta porque se absorbe calor del entorno. Esta propiedad es fundamental para comprender cómo las reacciones químicas afectan el equilibrio térmico de un sistema.
 Diferencia entre imbibición y ósmosis
Diferencia entre imbibición y ósmosisImportancia de la Entalpía
- Permite calcular el calor en reacciones químicas.
- Es esencial en procesos industriales como la refrigeración y la combustión.
- Ayuda en el diseño de sistemas energéticos eficientes.
- Es utilizada en estudios de equilibrio químico.
La entalpía también se utiliza en la ingeniería para diseñar sistemas térmicos y para calcular la eficiencia de máquinas térmicas, como motores y turbinas. Comprender cómo la entalpía se relaciona con el trabajo y el calor es esencial para cualquier ingeniero que trabaje en el campo de la energía. mientras que la entropía se ocupa del desorden y la dirección de los procesos, la entalpía se centra en la energía y el calor en los sistemas a presión constante.
Diferencias Clave entre Entropía y Entalpía
Aunque la entropía y la entalpía son conceptos fundamentales en la termodinámica, tienen diferencias clave que es importante entender. Una de las diferencias más significativas es que la entropía está relacionada con el desorden y la dirección de los procesos espontáneos, mientras que la entalpía está relacionada con la energía total de un sistema. La entropía se mide en joules por kelvin (J/K), mientras que la entalpía se mide en joules (J).
Otra diferencia importante es que la entropía es una función de estado que solo depende del estado actual del sistema, mientras que la entalpía puede cambiar durante un proceso a presión constante. En una reacción química, por ejemplo, la entalpía puede cambiar significativamente, mientras que la entropía puede ser más constante dependiendo de las condiciones del sistema. Esta distinción es fundamental para el análisis termodinámico de los procesos químicos y físicos.
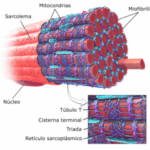 Diferencia entre miofibrillas y miofilamentos
Diferencia entre miofibrillas y miofilamentosComparación Visual
- Entropía: Medida del desorden, se relaciona con la dirección de los procesos.
- Entalpía: Medida de la energía total, se relaciona con el calor en reacciones.
- Entropía: Se mide en J/K, entalpía: se mide en J.
- Entropía: Función de estado, entalpía: puede cambiar durante procesos.
Además, la entropía es un concepto que se relaciona más con la probabilidad y la estadística, mientras que la entalpía se relaciona más con la energía y la termodinámica. En el estudio de reacciones químicas, por ejemplo, la entalpía nos dice cuánto calor se libera o se absorbe, mientras que la entropía nos ayuda a predecir si una reacción ocurrirá espontáneamente. Esta diferencia en el enfoque y la aplicación de ambos conceptos es crucial para comprender su importancia en la ciencia.
Ejemplos Prácticos de Entropía y Entalpía
Para ilustrar mejor la diferencia entre entropía y entalpía, consideremos algunos ejemplos prácticos. Imaginemos un sistema cerrado que contiene gas a temperatura y presión constantes. Si el gas se expande espontáneamente, la entropía del sistema aumentará porque hay más maneras de organizar las moléculas del gas en un volumen mayor. Este aumento en la entropía es un reflejo del aumento en el desorden del sistema.
Por otro lado, si consideramos una reacción química en la que se combinan reactivos para formar productos, la entalpía nos dirá si la reacción es exotérmica o endotérmica. Si se libera calor durante la reacción, la entalpía del sistema disminuirá. En este caso, la entalpía se convierte en una herramienta esencial para calcular el calor involucrado en el proceso, mientras que la entropía nos ayuda a entender la espontaneidad de la reacción.
Ejemplo de Entropía
- Expansión de un gas: Aumento de entropía.
- Mezcla de líquidos: Aumento de entropía.
- Fusión de un sólido: Aumento de entropía.
En el caso de la mezcla de líquidos, cuando dos líquidos diferentes se combinan, el sistema se vuelve más desordenado, lo que resulta en un aumento de la entropía. Este aumento es un indicador de que el sistema ha pasado a un estado más probable y desordenado. Similarmente, cuando un sólido se funde para convertirse en líquido, las moléculas en el líquido tienen más libertad de movimiento, lo que también resulta en un aumento de la entropía.
Ejemplo de Entalpía
- Reacción de combustión: Disminución de entalpía.
- Reacción de fotosíntesis: Aumento de entalpía.
- Evaporación del agua: Aumento de entalpía.
Un ejemplo común de un cambio en la entalpía es la reacción de combustión. En este proceso, el combustible se quema en presencia de oxígeno, liberando calor y disminuyendo la entalpía del sistema. Por otro lado, en la fotosíntesis, las plantas absorben energía solar para convertir dióxido de carbono y agua en glucosa y oxígeno, lo que resulta en un aumento de la entalpía. De igual manera, la evaporación del agua requiere energía, lo que también aumenta la entalpía del sistema.
Relación entre Entropía y Entalpía
Aunque la entropía y la entalpía son conceptos distintos, están interrelacionados en muchos aspectos de la termodinámica. Por ejemplo, la entropía y la entalpía están involucradas en la ecuación de Gibbs, que es fundamental para entender la espontaneidad de los procesos químicos. La ecuación de Gibbs se expresa como: ΔG = ΔH – TΔS, donde ΔG es el cambio en la energía libre de Gibbs, ΔH es el cambio en la entalpía, T es la temperatura en kelvins y ΔS es el cambio en la entropía.
Esta relación indica que la espontaneidad de un proceso depende no solo de la energía total (entalpía) sino también del desorden (entropía) en el sistema. Si el cambio en la entalpía es negativo (reacción exotérmica) y el cambio en la entropía es positivo, el proceso será espontáneo a cualquier temperatura. Por el contrario, si la entalpía es positiva y la entropía es negativa, el proceso no será espontáneo.
Ejemplos de Relación
- Reacciones exotérmicas: Entalpía negativa y entropía positiva = espontáneas.
- Reacciones endotérmicas: Entalpía positiva y entropía negativa = no espontáneas.
- Reacciones con entalpía cero: Cambios en entropía pueden determinar espontaneidad.
la relación entre la entropía y la entalpía es esencial para entender los procesos termodinámicos. Ambas propiedades se combinan para determinar la espontaneidad y el equilibrio de las reacciones químicas. Esto es especialmente relevante en el diseño de procesos industriales y en la investigación científica, donde el control de la energía y el desorden es fundamental para lograr resultados eficientes y sostenibles.
Aplicaciones de la Entropía y la Entalpía
Las aplicaciones de la entropía y la entalpía son vastas y se extienden a diversas disciplinas científicas y tecnológicas. En la química, estos conceptos son cruciales para entender las reacciones y los equilibrios. Los químicos utilizan la entalpía para calcular la cantidad de calor que se libera o se absorbe en una reacción, mientras que la entropía les ayuda a predecir si una reacción ocurrirá espontáneamente.
En la ingeniería, la entropía y la entalpía son fundamentales en el diseño de sistemas de energía, como centrales eléctricas y motores. Los ingenieros utilizan estos conceptos para maximizar la eficiencia de las máquinas térmicas y minimizar la pérdida de energía. Además, en la refrigeración y la climatización, se aplican principios termodinámicos que involucran la entropía y la entalpía para mantener temperaturas adecuadas en espacios cerrados.
Aplicaciones en Química
- Cálculo de calor en reacciones químicas.
- Predicción de la espontaneidad de reacciones.
- Estudio de equilibrios químicos.
En el campo de la biología, la entropía es relevante para entender procesos como la fotosíntesis y la respiración celular. Estos procesos implican transferencias de energía y cambios en la organización de la materia. La entalpía también se utiliza para estudiar la energía involucrada en la formación de biomoléculas, lo que es esencial para la investigación en bioquímica y biotecnología.
Aplicaciones en Ingeniería
- Diseño de sistemas de energía eficiente.
- Optimización de motores y turbinas.
- Control de procesos térmicos en refrigeración.
la entropía y la entalpía son conceptos fundamentales que tienen aplicaciones prácticas en múltiples campos. Su comprensión es esencial para cualquier profesional que trabaje en áreas relacionadas con la energía, la química, la biología y la ingeniería. Estos conceptos no solo ayudan a resolver problemas teóricos, sino que también son fundamentales para el desarrollo de tecnologías sostenibles y eficientes.
Conclusión sobre la Entropía y la Entalpía
A lo largo de este artículo, hemos explorado las diferencias y similitudes entre la entropía y la entalpía, así como sus aplicaciones en diversos campos de la ciencia y la ingeniería. Estos conceptos son fundamentales para entender los principios de la termodinámica y cómo se aplican en situaciones del mundo real. La entropía nos proporciona información sobre el desorden y la dirección de los procesos, mientras que la entalpía nos ayuda a comprender la energía involucrada en reacciones y cambios de estado.
Ambas propiedades son esenciales para el análisis de sistemas termodinámicos y tienen un impacto significativo en la investigación científica y el desarrollo tecnológico. Al comprender la relación entre la entropía y la entalpía, podemos abordar problemas complejos en química, biología e ingeniería, lo que nos permite avanzar hacia un futuro más eficiente y sostenible.
