La diferencia entre espectros de absorción y emisión es un tema fundamental en la física y la química, especialmente en el estudio de la luz y la materia. Ambos tipos de espectros se relacionan con la interacción de la luz con los átomos y moléculas, pero representan procesos opuestos. En este artículo, exploraremos en profundidad qué son estos espectros, cómo se forman y en qué se diferencian. Además, veremos su importancia en diversas aplicaciones científicas y tecnológicas.
¿Qué es un espectro de absorción?
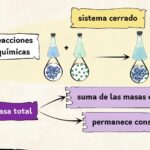 Diferencia entre la ley de conservación de la masa y la ley de proporción constante
Diferencia entre la ley de conservación de la masa y la ley de proporción constanteUn espectro de absorción se forma cuando un material, generalmente un gas o un líquido, absorbe luz en ciertas longitudes de onda. Cuando la luz blanca, que contiene todas las longitudes de onda del espectro visible, pasa a través de un material, algunos fotones son absorbidos por los electrones de los átomos o moléculas presentes en ese material. Este proceso provoca que los electrones se exciten y pasen a niveles de energía más altos.
El resultado es que el espectro de luz que emerge del material no es completo; faltan ciertas longitudes de onda. Estas longitudes de onda corresponden a las energías que los electrones han absorbido. En un gráfico, esto se representa como líneas oscuras en un fondo continuo de luz. Cada línea oscura corresponde a una longitud de onda específica que ha sido absorbida, lo que permite identificar los elementos presentes en el material.
Características del espectro de absorción
- Bandas de absorción: Las líneas en un espectro de absorción son conocidas como bandas de absorción. Cada banda corresponde a un elemento químico o a un compuesto específico.
- Condiciones necesarias: Para que se forme un espectro de absorción, debe haber una fuente de luz, un material que absorba la luz y un detector que registre la luz transmitida.
- Uso en análisis químicos: Los espectros de absorción son herramientas valiosas en la espectroscopía, que se utiliza para analizar la composición de sustancias.
¿Qué es un espectro de emisión?
Por otro lado, un espectro de emisión se genera cuando un material emite luz en ciertas longitudes de onda. Esto ocurre cuando los electrones en un átomo o molécula, que han sido excitados por calor o energía eléctrica, regresan a sus niveles de energía originales. Durante este proceso, liberan la energía en forma de fotones, que se manifiestan como luz visible o en otras longitudes de onda del espectro electromagnético.
El espectro de emisión se presenta como líneas brillantes en un fondo oscuro. Cada línea brillante representa una longitud de onda específica que ha sido emitida por el material. Al igual que en el caso del espectro de absorción, cada línea en el espectro de emisión corresponde a un elemento o compuesto específico, lo que permite su identificación. Este fenómeno es utilizado en diversas aplicaciones, desde la astronomía hasta la fabricación de dispositivos electrónicos.
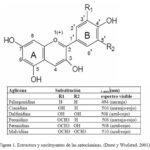 Diferencia entre antocianina y antocianidina
Diferencia entre antocianina y antocianidinaCaracterísticas del espectro de emisión
- Bandas de emisión: Las líneas en un espectro de emisión se conocen como bandas de emisión, y cada una corresponde a una transición electrónica particular.
- Condiciones necesarias: Para que se forme un espectro de emisión, es necesario un material excitado que pueda liberar energía en forma de luz.
- Aplicaciones en astronomía: Los espectros de emisión son cruciales en astronomía para identificar la composición química de estrellas y galaxias.
Principales diferencias entre espectros de absorción y emisión
Las diferencias entre un espectro de absorción y uno de emisión son fundamentales para entender cómo interactúan la luz y la materia. En primer lugar, la forma en que se generan estos espectros es opuesta. Mientras que un espectro de absorción se forma cuando un material absorbe ciertas longitudes de onda de luz, el espectro de emisión se produce cuando un material emite luz después de haber sido excitado. Esta es la diferencia más básica pero crucial entre ambos.
Además, el aspecto visual de cada espectro también es diferente. En un espectro de absorción, se observan líneas oscuras en un fondo continuo, mientras que en un espectro de emisión se ven líneas brillantes en un fondo oscuro. Estas características permiten a los científicos y técnicos identificar fácilmente qué tipo de espectro están analizando y, por ende, qué procesos están ocurriendo en el material en cuestión.
Otras diferencias importantes
- Origen de la luz: En el espectro de absorción, la luz proviene de una fuente externa, mientras que en el espectro de emisión, la luz es generada por el propio material.
- Aplicaciones prácticas: Los espectros de absorción se utilizan comúnmente en análisis químicos, mientras que los espectros de emisión son fundamentales en la astronomía y la física de plasmas.
- Información sobre el material: Ambos espectros proporcionan información sobre la composición química, pero lo hacen desde diferentes perspectivas; uno a través de la luz que se absorbe y el otro a través de la luz que se emite.
Aplicaciones de los espectros de absorción y emisión
Los espectros de absorción y emisión tienen numerosas aplicaciones en diversas áreas de la ciencia y la tecnología. En el campo de la química analítica, los espectros de absorción son herramientas esenciales para determinar la concentración de sustancias en una muestra. Por ejemplo, mediante la espectroscopía UV-Vis, se puede medir la cantidad de luz absorbida por una solución, lo que permite calcular la concentración de un compuesto específico.
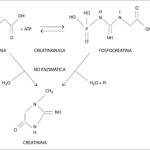 Diferencia entre creatina y creatinina
Diferencia entre creatina y creatininaEn la astronomía, los espectros de emisión son utilizados para estudiar la composición de estrellas y galaxias. Los astrónomos analizan la luz emitida por estos cuerpos celestes para identificar los elementos que los componen. Por ejemplo, la presencia de líneas espectrales de hidrógeno o helio puede indicar la composición de una estrella y su temperatura. Esto es vital para entender la evolución estelar y la formación de estructuras en el universo.
Otras aplicaciones relevantes
- Monitoreo ambiental: La espectroscopía de absorción se utiliza para medir contaminantes en el aire y el agua, lo que ayuda en la gestión ambiental.
- Diagnóstico médico: La espectroscopía se aplica en la medicina para analizar tejidos y fluidos corporales, facilitando diagnósticos precisos.
- Desarrollo de tecnología: La tecnología LED y láser se basa en principios de emisión de luz, mostrando la relevancia de estos espectros en la innovación tecnológica.
Ejemplos de espectros de absorción y emisión
Para entender mejor los conceptos de espectros de absorción y emisión, es útil considerar algunos ejemplos concretos. Un ejemplo clásico de un espectro de absorción es el espectro de absorción del cloro. Cuando se analiza la luz que pasa a través de una muestra de gas de cloro, se observarán líneas oscuras en el espectro donde el cloro ha absorbido luz en longitudes de onda específicas. Este tipo de análisis es crucial en laboratorios químicos para identificar la presencia de cloro en una mezcla.
En el caso de los espectros de emisión, un ejemplo común es el espectro de emisión del sodio. Cuando se calienta o se excita un gas de sodio, emite luz en longitudes de onda específicas que aparecen como líneas brillantes en el espectro. Estas líneas son características del sodio y pueden ser utilizadas para identificar su presencia en diversas muestras. Este fenómeno es utilizado en la fabricación de lámparas de vapor de sodio, que son muy comunes en la iluminación pública.
Importancia de los ejemplos
- Identificación de sustancias: Los ejemplos de espectros ayudan a ilustrar cómo se pueden identificar sustancias en diferentes contextos.
- Desarrollo de tecnologías: La comprensión de estos espectros ha llevado al desarrollo de tecnologías que utilizan luz de manera eficiente.
- Investigación científica: Estos ejemplos son fundamentales para la investigación en diversas disciplinas científicas, desde la química hasta la astronomía.
Instrumentos utilizados para medir espectros
La medición de espectros de absorción y emisión se lleva a cabo utilizando instrumentos específicos que pueden analizar la luz en diferentes longitudes de onda. Uno de los instrumentos más comunes es el espectrómetro, que se utiliza para dispersar la luz y registrar las longitudes de onda presentes en un espectro. Estos dispositivos pueden ser utilizados en laboratorios para realizar análisis detallados de sustancias químicas y biológicas.
Existen diferentes tipos de espectrómetros, incluyendo espectrómetros de masa, espectrómetros de absorción y espectrómetros de emisión. Cada uno de estos instrumentos está diseñado para aplicaciones específicas y utiliza principios de óptica y fotónica para realizar sus mediciones. Por ejemplo, un espectrómetro de masas se utiliza para analizar la composición de moléculas, mientras que un espectrómetro de absorción se centra en medir la luz absorbida por una muestra.
Tipos de instrumentos
- Espectrómetros de absorción: Miden la luz que es absorbida por una muestra, permitiendo determinar la concentración de diferentes sustancias.
- Espectrómetros de emisión: Detectan la luz emitida por un material excitado, lo que es útil para identificar elementos y compuestos.
- Espectrofotómetros: Son instrumentos que miden la intensidad de la luz en diferentes longitudes de onda, facilitando el análisis espectral.
Desafíos en el análisis espectral
A pesar de la utilidad de los espectros de absorción y emisión, existen desafíos en el análisis espectral que los científicos deben tener en cuenta. Uno de los principales desafíos es la interferencia de otras sustancias en la muestra. En ocasiones, la presencia de impurezas puede afectar las mediciones, dificultando la identificación precisa de los compuestos. Por lo tanto, es fundamental realizar un análisis cuidadoso y, en algunos casos, purificar las muestras antes de llevar a cabo el análisis espectral.
Otro desafío es la resolución espectral. La resolución espectral se refiere a la capacidad de un instrumento para distinguir entre longitudes de onda cercanas. Un espectrómetro de baja resolución puede no ser capaz de detectar líneas espectrales que están muy próximas entre sí, lo que puede llevar a conclusiones erróneas sobre la composición de una muestra. Por lo tanto, la elección del instrumento adecuado y la calibración precisa son aspectos críticos en el análisis espectral.
Más desafíos en el análisis
- Condiciones ambientales: Factores como temperatura y presión pueden afectar las mediciones espectrales, lo que requiere un control riguroso del entorno de análisis.
- Limitaciones tecnológicas: No todos los espectrómetros son igualmente precisos; algunos pueden ser costosos y requieren capacitación especializada para su uso.
- Interpretación de datos: La interpretación de los datos espectrales puede ser compleja y requiere experiencia en el campo para evitar errores.
Futuro de la espectroscopía
El futuro de la espectroscopía, que incluye tanto los espectros de absorción como los de emisión, parece prometedor. Con el avance de la tecnología, los instrumentos están mejorando en precisión y capacidad de análisis. Por ejemplo, se están desarrollando espectrómetros más compactos y portátiles que permiten realizar análisis en el campo, lo que amplía las aplicaciones en áreas como la agricultura y la medicina.
Además, la inteligencia artificial y el aprendizaje automático están comenzando a desempeñar un papel en la interpretación de datos espectrales. Estas tecnologías pueden ayudar a procesar grandes volúmenes de datos y a identificar patrones que podrían pasar desapercibidos para el ojo humano. Esto no solo mejorará la precisión de los análisis, sino que también acelerará el proceso de identificación y caracterización de compuestos.
Innovaciones en espectroscopía
- Espectroscopía en tiempo real: Nuevas técnicas permiten realizar análisis espectrales en tiempo real, lo que es útil en aplicaciones industriales y de investigación.
- Espectroscopía de imágenes: Combina imágenes y espectroscopía para analizar la composición de superficies complejas de manera más detallada.
- Aplicaciones biotecnológicas: La espectroscopía está siendo utilizada para desarrollar nuevos métodos de diagnóstico y tratamiento en medicina personalizada.
los espectros de absorción y emisión son fundamentales para entender la interacción entre la luz y la materia. Aunque tienen diferencias clave en su formación y apariencia, ambos tipos de espectros son herramientas valiosas en diversas aplicaciones científicas y tecnológicas. A medida que la tecnología avanza, es probable que veamos un desarrollo continuo en el campo de la espectroscopía, lo que permitirá a los científicos explorar aún más los misterios del universo.
