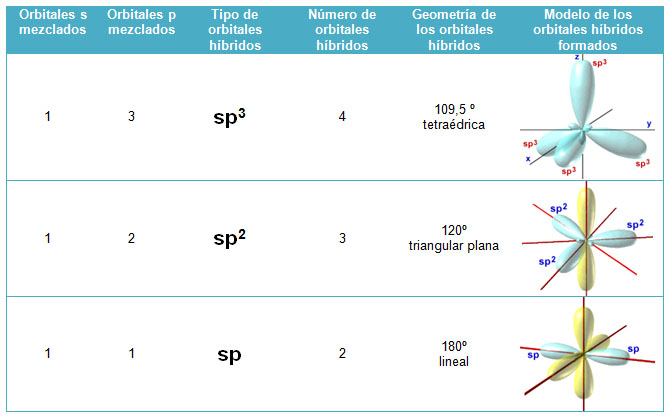
La hibridación es un concepto fundamental en la química que describe cómo los átomos se combinan para formar enlaces químicos. En particular, la hibridación sp2 y sp3 son dos tipos de hibridación que se encuentran comúnmente en compuestos orgánicos. Estas configuraciones afectan tanto la geometría molecular como las propiedades físicas y químicas de las moléculas. A continuación, exploraremos en detalle las diferencias entre la hibridación sp2 y sp3, analizando sus características, ejemplos y la importancia que tienen en la química.
Características de la hibridación sp2
La hibridación sp2 ocurre cuando un átomo de carbono se combina con otros dos átomos o grupos de átomos, formando tres orbitales híbridos. En este proceso, un orbital s y dos orbitales p se combinan para crear tres orbitales sp2 equivalentes. Cada uno de estos orbitales forma un enlace sigma, lo que resulta en una geometría trigonal plana con un ángulo de enlace de aproximadamente 120 grados. Esta configuración es común en compuestos que contienen dobles enlaces, como el etileno.
La presencia de un doble enlace en la hibridación sp2 también implica que hay un orbital p no hibridado que queda disponible. Este orbital p se utiliza para formar un enlace pi, que es esencial para la formación de compuestos insaturados. En resumen, la hibridación sp2 no solo determina la forma de la molécula, sino que también influye en su reactividad y propiedades químicas.
 Diferencia entre dextrina y maltodextrina
Diferencia entre dextrina y maltodextrinaEjemplos de hibridación sp2
- Etileno (C2H4): Este es uno de los ejemplos más simples de la hibridación sp2. En el etileno, cada carbono está unido a otros dos átomos de carbono y a dos átomos de hidrógeno, formando un doble enlace entre los carbonos.
- Acetona (C3H6O): En la acetona, el carbono central está hibridado como sp2, formando enlaces con dos grupos metilo y un grupo carbonilo.
- Fosfina (PH3): Aunque menos común, la fosfina también puede presentar hibridación sp2 en ciertas condiciones, donde el fósforo forma enlaces con tres átomos de hidrógeno.
Características de la hibridación sp3
La hibridación sp3 se produce cuando un átomo de carbono se une a otros cuatro átomos o grupos de átomos. En este caso, un orbital s y tres orbitales p se combinan para formar cuatro orbitales sp3 equivalentes. Cada uno de estos orbitales híbridos se utiliza para formar un enlace sigma, lo que resulta en una geometría tetraédrica con un ángulo de enlace de aproximadamente 109.5 grados. Esta configuración es común en compuestos saturados, como el metano.
La hibridación sp3 implica que todos los enlaces son enlaces simples, lo que significa que no hay enlaces dobles o triples presentes. Esto resulta en una mayor estabilidad en comparación con los compuestos que contienen hibridación sp2 o sp. La estructura tetraédrica también permite una distribución más uniforme de los electrones alrededor del núcleo del átomo, lo que contribuye a la estabilidad de la molécula.
Ejemplos de hibridación sp3
- Metano (CH4): Este es el ejemplo más clásico de hibridación sp3. En el metano, el carbono forma cuatro enlaces simples con cuatro átomos de hidrógeno.
- Etano (C2H6): En el etano, cada carbono está hibridado como sp3 y forma enlaces simples con otros carbonos y átomos de hidrógeno.
- Amoniaco (NH3): El nitrógeno en el amoniaco también está hibridado como sp3, formando tres enlaces con átomos de hidrógeno y un par de electrones no compartidos.
Diferencias clave entre hibridación sp2 y sp3
Una de las diferencias más evidentes entre la hibridación sp2 y sp3 es la cantidad de enlaces que pueden formar. En la hibridación sp2, el carbono puede formar un doble enlace debido a la presencia del orbital p no hibridado. Esto no es posible en la hibridación sp3, donde solo se forman enlaces simples. Esta diferencia en la capacidad de enlace afecta directamente las propiedades químicas y físicas de las moléculas.
 Diferencia entre la bilis hepática y la bilis de la vesícula biliar
Diferencia entre la bilis hepática y la bilis de la vesícula biliarOtra diferencia clave es la geometría de las moléculas resultantes. Las moléculas con hibridación sp2 tienen una geometría trigonal plana, lo que les confiere propiedades únicas, como la reactividad en reacciones de adición. Por otro lado, las moléculas con hibridación sp3 tienen una geometría tetraédrica, lo que les proporciona una mayor estabilidad y menos reactividad. Esta estabilidad es una de las razones por las cuales los compuestos saturados son más comunes en la naturaleza.
Comparación de ángulos de enlace
- Los ángulos de enlace en la hibridación sp2 son aproximadamente 120 grados.
- Los ángulos de enlace en la hibridación sp3 son aproximadamente 109.5 grados.
Propiedades físicas y químicas
Las diferencias en la hibridación también afectan las propiedades físicas y químicas de los compuestos. Los compuestos hibridados como sp2 suelen ser más reactivos debido a la presencia de enlaces dobles, que son más susceptibles a reacciones químicas. Por ejemplo, en la química orgánica, los compuestos insaturados, como los alquenos y los alquinos, son utilizados en diversas reacciones de adición, donde otros átomos o grupos se añaden a la molécula.
 Diferencia entre oligosacáridos y polisacáridos
Diferencia entre oligosacáridos y polisacáridosPor otro lado, los compuestos con hibridación sp3 tienden a ser más estables y menos reactivos. Esto se debe a que sus enlaces simples son más fuertes y requieren más energía para romperse. Por esta razón, los compuestos saturados son comúnmente encontrados en la naturaleza, como en los hidrocarburos que se encuentran en el petróleo y el gas natural.
Influencia en la polaridad de las moléculas
- Las moléculas hibridadas como sp2 pueden ser polares o no polares, dependiendo de la disposición de los grupos alrededor del carbono.
- Las moléculas hibridadas como sp3 son generalmente más polares debido a la presencia de pares de electrones no compartidos, como en el amoniaco.
Aplicaciones en la química orgánica
La comprensión de la hibridación sp2 y sp3 es esencial en la química orgánica, donde se estudian las estructuras y reacciones de compuestos que contienen carbono. Los químicos utilizan este conocimiento para predecir cómo se comportarán las moléculas en diferentes condiciones. Por ejemplo, al diseñar fármacos, es importante considerar la hibridación para optimizar la actividad biológica y la solubilidad de los compuestos.
Además, la hibridación también juega un papel crucial en la síntesis de nuevos materiales. Los científicos pueden manipular la hibridación de los átomos de carbono para crear polímeros con propiedades específicas, como la flexibilidad o la resistencia. Esto es especialmente relevante en el desarrollo de nuevos plásticos y materiales compuestos que se utilizan en diversas aplicaciones industriales.
Impacto en la biología
- Las moléculas biológicas, como los aminoácidos y los ácidos nucleicos, a menudo presentan hibridación sp2 y sp3, lo que afecta su estructura y función.
- La hibridación influye en la forma en que las enzimas interactúan con sus sustratos, lo que es crucial para la biología celular.
Conclusiones sobre hibridación sp2 y sp3
La hibridación sp2 y sp3 son conceptos fundamentales que permiten entender cómo los átomos de carbono se combinan para formar una variedad de compuestos. Estas configuraciones afectan la geometría molecular, los ángulos de enlace y las propiedades físicas y químicas de las moléculas. Conocer las diferencias entre estas dos formas de hibridación es crucial para cualquier persona interesada en la química, la biología y la ciencia de materiales.
A través de ejemplos prácticos y aplicaciones en la vida real, podemos apreciar la importancia de la hibridación en la comprensión de la química y su relevancia en diversas áreas de la ciencia. La hibridación sp2 y sp3 no solo son términos técnicos, sino que representan principios que rigen la naturaleza misma de las moléculas y sus interacciones en el mundo que nos rodea.