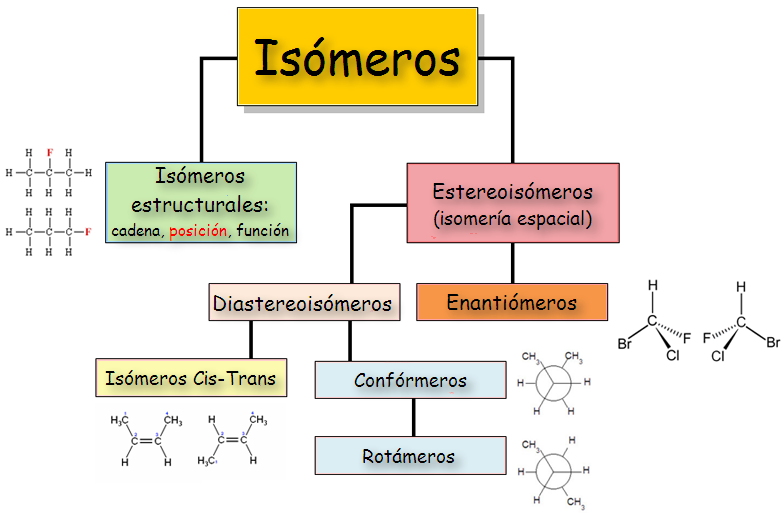
La química orgánica es un campo fascinante que se ocupa de la estructura, propiedades y reacciones de los compuestos que contienen carbono. Uno de los conceptos clave en esta disciplina son los isómeros, que son compuestos que tienen la misma fórmula molecular pero diferentes disposiciones de sus átomos. Dentro de los isómeros, podemos encontrar dos categorías principales: los isómeros geométricos y los isómeros estructurales. Aunque ambos tipos de isómeros comparten características similares, tienen diferencias fundamentales que afectan su comportamiento y propiedades. En este artículo, exploraremos estas diferencias en detalle, comenzando por la definición de cada tipo de isómero.
Definición de Isómeros
Los isómeros son compuestos que, a pesar de tener la misma fórmula química, presentan estructuras diferentes. Esta variación en la estructura puede influir en las propiedades físicas y químicas de los compuestos. Existen varios tipos de isómeros, pero aquí nos centraremos en dos categorías principales: los isómeros geométricos y los isómeros estructurales. Cada tipo tiene su propio conjunto de características y ejemplos que los hacen únicos. Para comprender mejor estas diferencias, es importante analizar cada tipo de isómero en profundidad.
Isómeros Estructurales
Los isómeros estructurales son compuestos que tienen la misma fórmula molecular, pero sus átomos están conectados de manera diferente. Esta diferencia en la conexión de los átomos se traduce en variaciones en la estructura del compuesto, lo que puede afectar su reactividad y propiedades. Existen varios tipos de isómeros estructurales, que incluyen los isómeros de cadena, los isómeros de posición y los isómeros funcionales.
 Diferencia entre aromático antiaromático y no aromático
Diferencia entre aromático antiaromático y no aromáticoIsómeros de Cadena
Los isómeros de cadena son aquellos que difieren en la forma en que los átomos de carbono están organizados en una cadena. Por ejemplo, el butano (C4H10) puede existir en dos formas: el butano lineal y el isobutano, que tiene una estructura ramificada. Esta diferencia en la estructura de la cadena puede afectar las propiedades físicas, como el punto de ebullición y la densidad del compuesto.
Isómeros de Posición
Los isómeros de posición se forman cuando el grupo funcional de un compuesto se encuentra en diferentes posiciones dentro de la misma cadena de carbono. Por ejemplo, el alcohol butílico puede presentarse como butanol en la posición uno o en la posición dos de la cadena. A pesar de tener la misma fórmula molecular, las propiedades de estos compuestos pueden variar considerablemente debido a la ubicación del grupo funcional.
 Diferencia entre células madre mesenquimales y hematopoyéticas
Diferencia entre células madre mesenquimales y hematopoyéticasIsómeros Funcionales
Los isómeros funcionales son aquellos que tienen diferentes grupos funcionales, lo que les confiere propiedades químicas distintas. Por ejemplo, el etanol (un alcohol) y el etileno (un alceno) son isómeros funcionales. A pesar de compartir la misma fórmula molecular (C2H6O), su comportamiento químico es completamente diferente debido a la naturaleza de sus grupos funcionales.
Isómeros Geométricos
Los isómeros geométricos, también conocidos como isómeros cis-trans, son compuestos que tienen la misma fórmula molecular y la misma conexión de átomos, pero difieren en la disposición espacial de los átomos. Este tipo de isomería se presenta principalmente en compuestos que tienen dobles enlaces o en ciclos, donde la rotación alrededor del enlace está restringida. Los isómeros geométricos pueden tener diferentes propiedades físicas y químicas, lo que los hace importantes en la química orgánica.
Isómeros Cis y Trans
En los isómeros cis y trans, la diferencia se basa en la posición de los grupos en relación con el doble enlace o el ciclo. En los isómeros cis, los grupos similares están en el mismo lado del doble enlace o del ciclo, mientras que en los isómeros trans, están en lados opuestos. Por ejemplo, en el buteno, si ambos grupos metilo (CH3) están en el mismo lado, se considera un isómero cis; si están en lados opuestos, es un isómero trans. Esta diferencia puede influir en las propiedades físicas, como el punto de ebullición y la solubilidad.
 Diferencia entre valencia y estado de oxidación
Diferencia entre valencia y estado de oxidaciónImpacto en Propiedades Físicas
La disposición espacial de los átomos en los isómeros geométricos tiene un impacto significativo en sus propiedades físicas. Por ejemplo, los isómeros cis tienden a tener puntos de ebullición más altos que sus contrapartes trans debido a que su forma les permite formar enlaces de hidrógeno más efectivos. Esta diferencia en las propiedades puede ser crucial en aplicaciones industriales y en la naturaleza, donde la forma de la molécula puede determinar su función biológica.
Diferencias Clave entre Isómeros Geométricos y Estructurales
Ahora que hemos explorado las definiciones y ejemplos de ambos tipos de isómeros, es fundamental resaltar las diferencias clave entre los isómeros geométricos y los isómeros estructurales. Estas diferencias no solo son teóricas, sino que también tienen implicaciones prácticas en el mundo real, especialmente en la química orgánica y la biología.
Conexión de Átomos
Una de las diferencias más evidentes entre los isómeros geométricos y estructurales radica en cómo están conectados los átomos. En los isómeros estructurales, la conexión de los átomos es diferente, lo que significa que los compuestos pueden tener diferentes cadenas de carbono o diferentes posiciones de grupos funcionales. En cambio, los isómeros geométricos tienen la misma conexión de átomos, pero varían en la disposición espacial de esos átomos. Esta diferencia en la conexión de átomos es fundamental para entender cómo se comportan los compuestos.
Impacto en Propiedades
Las propiedades físicas y químicas de los compuestos pueden verse afectadas por el tipo de isómero que se esté considerando. Los isómeros estructurales pueden presentar diferencias significativas en sus puntos de ebullición, solubilidad y reactividad química, debido a la variación en la estructura. Por otro lado, los isómeros geométricos también presentan diferencias en propiedades físicas, pero estas son a menudo más sutiles y están relacionadas con la forma en que los grupos están dispuestos en el espacio. Esta variabilidad en las propiedades es un factor crucial en la aplicación de estos compuestos en diferentes campos.
Ejemplos Prácticos de Isómeros
Para ilustrar mejor la diferencia entre los isómeros geométricos y los isómeros estructurales, es útil considerar ejemplos específicos de cada tipo. A continuación, se presentan algunos ejemplos que destacan estas diferencias y sus implicaciones en la química.
Ejemplo de Isómeros Estructurales
Un buen ejemplo de isómeros estructurales es el caso del alcohol butílico. Este compuesto puede existir en varias formas: el butanol, el isobutanol y el sec-butanol. Cada uno de estos isómeros tiene la misma fórmula molecular (C4H10O), pero difieren en la disposición de sus átomos. Estas diferencias estructurales afectan su solubilidad y reactividad, lo que es crucial en aplicaciones industriales, como la producción de combustibles y solventes.
Ejemplo de Isómeros Geométricos
Un ejemplo clásico de isómeros geométricos es el 2-buteno. Este compuesto tiene dos formas: el isómero cis, donde los grupos metilo están en el mismo lado del doble enlace, y el isómero trans, donde los grupos metilo están en lados opuestos. Esta diferencia en la disposición espacial no solo afecta las propiedades físicas, como el punto de ebullición, sino que también puede influir en la forma en que el compuesto interactúa con otros reactivos en reacciones químicas.
Aplicaciones de los Isómeros en la Química y la Biología
La comprensión de los isómeros es fundamental en diversos campos de la química y la biología. La forma en que los átomos están organizados y dispuestos puede influir en la función biológica de las moléculas, así como en su reactividad química. Esto tiene implicaciones significativas en el desarrollo de fármacos, la síntesis de materiales y la comprensión de procesos biológicos.
Desarrollo de Fármacos
En la industria farmacéutica, la isomería juega un papel crucial. Muchos medicamentos son isómeros de un compuesto, y la forma en que están organizados puede determinar su eficacia y seguridad. Por ejemplo, el ibuprofeno tiene isómeros que pueden tener diferentes niveles de actividad biológica. Por lo tanto, la selección de un isómero específico puede ser fundamental para el desarrollo de un fármaco eficaz y seguro.
Biología Molecular
En biología, los isómeros también son importantes. Las moléculas biológicas, como los azúcares y los aminoácidos, pueden existir en diferentes formas isoméricas. Estas diferencias pueden influir en cómo las moléculas interactúan entre sí y en su función en procesos biológicos. Por ejemplo, la glucosa y la fructosa son isómeros que tienen la misma fórmula molecular, pero sus estructuras diferentes les confieren propiedades y funciones distintas en el metabolismo.
Resumen de las Diferencias entre Isómeros
los isómeros geométricos y los isómeros estructurales son dos categorías importantes de isómeros en química. Mientras que los isómeros estructurales difieren en la conexión de los átomos, los isómeros geométricos se diferencian en la disposición espacial de los mismos átomos. Ambas categorías tienen implicaciones significativas en las propiedades físicas y químicas de los compuestos, así como en su aplicación en campos como la farmacología y la biología. La comprensión de estas diferencias es crucial para cualquier persona interesada en el estudio de la química orgánica y sus aplicaciones prácticas.