La química y la física nuclear son campos fascinantes que estudian las propiedades de los átomos y sus interacciones. Dentro de estos estudios, dos conceptos importantes son los isótopos y las isobaras. Aunque ambos términos se relacionan con los átomos y sus núcleos, se refieren a diferentes aspectos de la estructura atómica. A continuación, exploraremos en profundidad las características, propiedades y diferencias entre isótopos e isobaras, así como su importancia en la ciencia y la tecnología.
Definición de isótopos
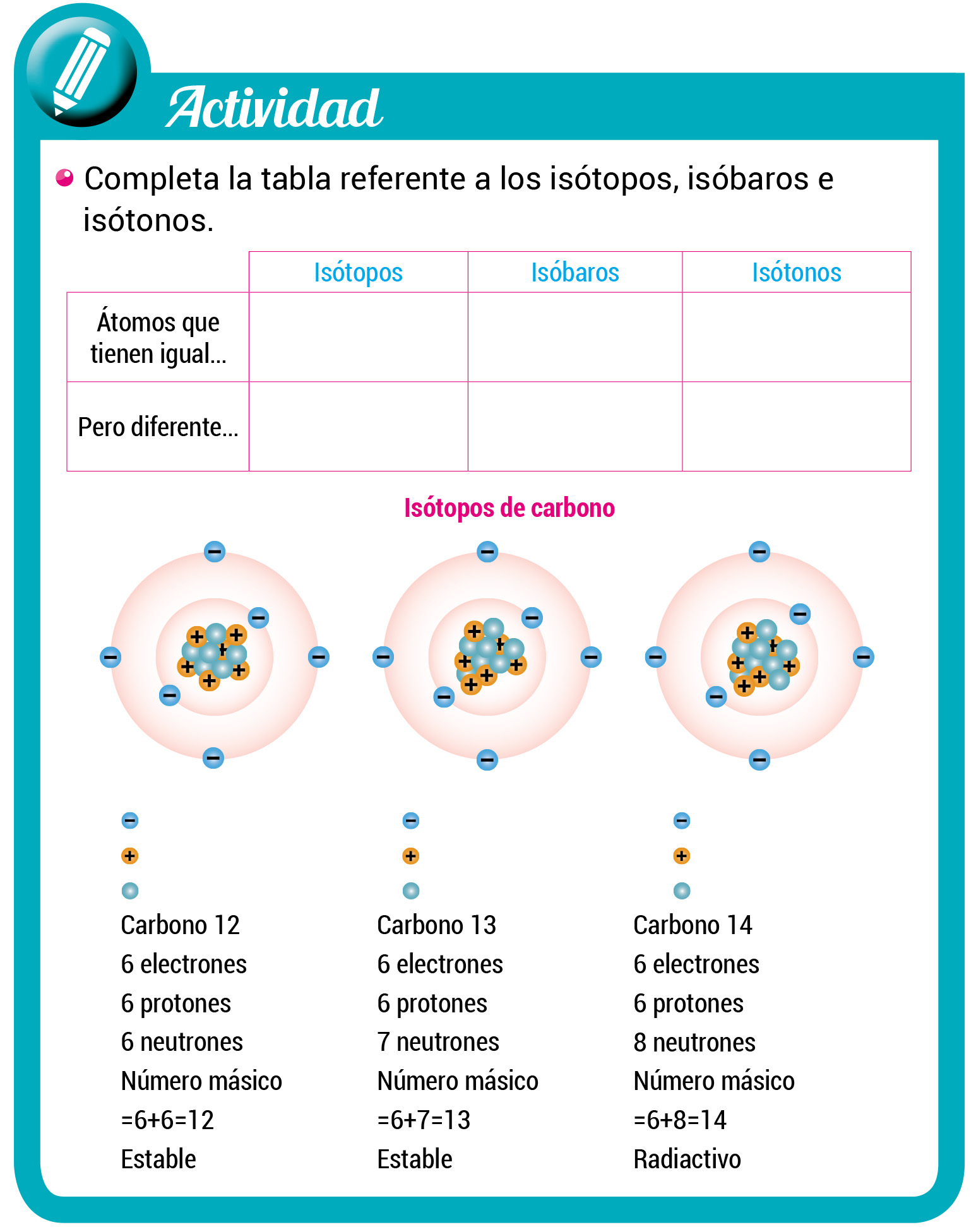
Los isótopos son variantes de un mismo elemento químico que tienen el mismo número de protones en el núcleo, pero diferente número de neutrones. Esto significa que los isótopos de un elemento tienen la misma configuración electrónica y, por lo tanto, comparten propiedades químicas similares. Sin embargo, su masa atómica varía debido a la diferencia en el número de neutrones. Por ejemplo, el carbono tiene varios isótopos, siendo el más común el carbono-12, que tiene 6 neutrones, y el carbono-14, que tiene 8 neutrones.
Es interesante notar que, aunque los isótopos de un mismo elemento se comportan químicamente de manera similar, sus propiedades físicas pueden diferir. Esto se debe a la diferencia en su masa atómica. Por ejemplo, el carbono-12 y el carbono-14 tienen diferentes puntos de fusión y ebullición, lo que puede ser útil en diversas aplicaciones científicas, como la datación por radiocarbono. En este proceso, se utiliza la cantidad de carbono-14 en un organismo para determinar su edad.
 Diferencia entre células mieloides y linfoides
Diferencia entre células mieloides y linfoidesTipos de isótopos
- Isótopos estables: No experimentan desintegración radiactiva y permanecen constantes a lo largo del tiempo.
- Isótopos radiactivos: Son inestables y se descomponen con el tiempo, emitiendo radiación en el proceso. Estos isótopos se utilizan en medicina y en la industria.
Los isótopos estables, como el carbono-12 y el oxígeno-16, son importantes en la biología y la ecología, ya que se encuentran en organismos vivos y en compuestos biológicos. Por otro lado, los isótopos radiactivos, como el uranio-238 y el carbono-14, son fundamentales en aplicaciones de energía nuclear y en la medicina para tratamientos de cáncer, donde se utilizan para localizar y destruir células cancerosas.
Definición de isobaras
Las isobaras, por otro lado, son átomos que tienen el mismo número de masa, es decir, la misma suma de protones y neutrones en sus núcleos, pero pertenecen a elementos diferentes. Esto significa que los isóbaros tienen diferentes números de protones, lo que les confiere propiedades químicas distintas. Por ejemplo, el carbono-14 y el nitrógeno-14 son isobaras, ya que ambos tienen una masa atómica de 14, pero el carbono tiene 6 protones y el nitrógeno tiene 7.
La existencia de isobaras es un fenómeno interesante en la química nuclear. La diversidad de isóbaras muestra cómo los átomos pueden variar en su composición nuclear y cómo estas variaciones afectan sus propiedades. Aunque los isóbaras tienen la misma masa, su comportamiento químico es diferente debido a su distinta cantidad de protones, lo que afecta su reactividad y su capacidad para formar enlaces químicos.
 Diferencia entre nailon y poliéster
Diferencia entre nailon y poliésterEjemplos de isobaras
- Carbono-14: Con 6 protones y 8 neutrones.
- Nitrógeno-14: Con 7 protones y 7 neutrones.
- Argón-40: Con 18 protones y 22 neutrones.
- Calcio-40: Con 20 protones y 20 neutrones.
Estos ejemplos muestran cómo diferentes elementos pueden compartir la misma masa atómica a través de diferentes combinaciones de protones y neutrones. Las isobaras son un área de estudio interesante en la física nuclear, ya que la comprensión de su comportamiento puede ayudar a los científicos a desentrañar la naturaleza de las reacciones nucleares y los procesos de desintegración.
Diferencias clave entre isótopos e isobaras
La principal diferencia entre isótopos e isobaras radica en el número de protones y neutrones en sus núcleos. Mientras que los isótopos tienen el mismo número de protones pero diferente número de neutrones, las isobaras tienen el mismo número de masa (protones más neutrones) pero pertenecen a elementos diferentes. Esta diferencia fundamental tiene implicaciones significativas en sus propiedades químicas y físicas.
Además, los isótopos pueden ser estables o radiactivos, mientras que las isobaras son, por definición, diferentes elementos y, por lo tanto, pueden tener características muy distintas. Por ejemplo, el carbono-14, que es un isótopo radiactivo, se utiliza en la datación de fósiles, mientras que el nitrógeno-14, que es un isótopo estable, es un componente esencial del aire que respiramos. Estas diferencias subrayan la importancia de comprender tanto los isótopos como las isobaras en el contexto de la química y la física.
 Diferencia entre la ósmosis inversa y el agua destilada
Diferencia entre la ósmosis inversa y el agua destiladaPropiedades físicas y químicas
Las propiedades físicas y químicas de los isótopos y las isobaras también son diferentes. Los isótopos, aunque pertenecen al mismo elemento, pueden mostrar diferencias en su densidad, punto de fusión y punto de ebullición. Estas variaciones son particularmente notables en los isótopos radiactivos, que pueden descomponerse y emitir radiación, afectando su estabilidad y comportamiento. Por otro lado, las isobaras, al ser diferentes elementos, tienen diferentes propiedades químicas y reactividades, lo que significa que pueden participar en reacciones químicas de maneras muy distintas.
Por ejemplo, mientras que el carbono-12 y el carbono-14 pueden reaccionar con oxígeno para formar dióxido de carbono, el nitrógeno-14 no puede participar en esta reacción de la misma manera, ya que su estructura atómica es diferente. Esto ilustra cómo la comprensión de isótopos e isobaras es crucial para la predicción del comportamiento de los elementos en diversas reacciones químicas y en aplicaciones industriales.
Aplicaciones de isótopos
Los isótopos tienen una amplia gama de aplicaciones en diversos campos, incluyendo la medicina, la arqueología, la agricultura y la energía. En medicina, los isótopos radiactivos se utilizan en diagnósticos y tratamientos. Por ejemplo, el yodo-131 se utiliza en el tratamiento de enfermedades de la tiroides, mientras que el tecnecio-99m es ampliamente utilizado en estudios de imágenes médicas, como escaneos de órganos.
En arqueología, los isótopos de carbono son esenciales para la datación de restos orgánicos. La técnica de datación por radiocarbono se basa en la medición de la cantidad de carbono-14 presente en un objeto para determinar su antigüedad. Esta técnica ha permitido a los científicos reconstruir la historia de civilizaciones antiguas y comprender mejor el pasado humano.
Otras aplicaciones de isótopos
- Investigación científica: Los isótopos se utilizan para rastrear procesos biogeoquímicos en ecosistemas.
- Industria: Se utilizan en la detección de fugas y en la medición de flujos en procesos industriales.
- Seguridad alimentaria: Los isótopos ayudan a identificar la procedencia de alimentos y a verificar su autenticidad.
La versatilidad de los isótopos en diversas aplicaciones demuestra su importancia en la ciencia y la tecnología. Estos elementos no solo ayudan a mejorar la calidad de vida a través de avances médicos, sino que también contribuyen a nuestra comprensión del mundo y del universo en general.
Aplicaciones de isobaras
Las aplicaciones de las isobaras son menos comunes en comparación con las de los isótopos, pero también tienen su relevancia. En la investigación nuclear, las isobaras pueden ser objeto de estudio para entender mejor las interacciones nucleares y la estabilidad de los núcleos atómicos. Por ejemplo, el estudio de las reacciones nucleares que involucran isobaras puede proporcionar información valiosa sobre la formación de elementos en las estrellas y los procesos de nucleosíntesis.
Además, en el campo de la física de partículas, las isobaras pueden ser analizadas para entender las fuerzas fundamentales que rigen el comportamiento de la materia a nivel subatómico. Esto puede llevar a descubrimientos sobre cómo se forman y descomponen los núcleos, así como sobre las propiedades de la materia en condiciones extremas.
Ejemplos de investigación con isobaras
- Física nuclear: Estudio de reacciones nucleares y su relación con la estabilidad de los núcleos.
- Astrofísica: Comprensión de la formación de elementos en el interior de las estrellas.
- Investigación de materiales: Uso de isobaras para analizar la composición de materiales y su comportamiento bajo diferentes condiciones.
Aunque las aplicaciones de las isobaras no son tan ampliamente reconocidas como las de los isótopos, su estudio es esencial para avanzar en la comprensión de la física nuclear y de los procesos que dan forma a nuestro universo. A medida que la tecnología avanza, es probable que se descubran nuevas aplicaciones para las isobaras, ampliando aún más nuestro conocimiento sobre la materia y la energía.
Relación entre isótopos e isobaras
A pesar de sus diferencias, los isótopos e isobaras están intrínsecamente relacionados en el contexto de la química y la física. Ambos conceptos giran en torno a la estructura atómica y a la forma en que los átomos se comportan en diferentes condiciones. La comprensión de estos dos tipos de átomos permite a los científicos predecir y explicar una amplia gama de fenómenos naturales y artificiales.
Por ejemplo, al estudiar la desintegración de un isótopo radiactivo, es posible que se produzcan isóbaras como productos de descomposición. Esto significa que el estudio de los isótopos no solo proporciona información sobre el elemento original, sino también sobre los nuevos elementos que pueden formarse a partir de su descomposición. Este fenómeno es fundamental en la investigación de procesos nucleares y en la comprensión de cómo se forman nuevos elementos en la naturaleza.
Interacciones en reacciones nucleares
Las reacciones nucleares que involucran isótopos e isobaras son un área de estudio activa en la física nuclear. Al observar cómo interactúan estos átomos, los científicos pueden obtener información sobre la fuerza nuclear y la estabilidad de los núcleos. Por ejemplo, en ciertas reacciones de fisión y fusión, los isótopos pueden transformarse en isobaras, liberando una gran cantidad de energía en el proceso.
Además, la investigación sobre isótopos e isobaras también ayuda a los científicos a entender fenómenos como la radiactividad y la fusión nuclear, que son fundamentales para el desarrollo de tecnologías de energía nuclear. La capacidad de manipular y comprender estos procesos tiene implicaciones significativas para la producción de energía y la seguridad nuclear.
Futuro de la investigación en isótopos e isobaras
El futuro de la investigación en isótopos e isobaras es prometedor, ya que la ciencia avanza a pasos agigantados. Nuevas tecnologías, como la espectrometría de masas y la tomografía por emisión de positrones (PET), están permitiendo a los científicos explorar estos conceptos de manera más profunda y precisa. Esto no solo enriquecerá nuestro conocimiento sobre la estructura atómica, sino que también abrirá nuevas oportunidades para aplicaciones prácticas en diversos campos.
Además, la investigación sobre isótopos radiactivos en el contexto del tratamiento del cáncer sigue siendo un área de gran interés. A medida que se desarrollan nuevos isótopos y técnicas de aplicación, es posible que se logren tratamientos más efectivos y menos invasivos para los pacientes. La exploración de isótopos en el ámbito de la medicina personalizada también promete revolucionar la forma en que abordamos diversas enfermedades.
Desarrollo de nuevas tecnologías
- Espectrometría de masas: Herramienta clave para la identificación y análisis de isótopos.
- Imágenes médicas avanzadas: Uso de isótopos radiactivos para diagnósticos más precisos.
- Investigación en energía nuclear: Nuevos métodos para mejorar la eficiencia y seguridad de las reacciones nucleares.
El desarrollo continuo de nuevas tecnologías y métodos de investigación promete llevar la comprensión de isótopos e isobaras a un nuevo nivel, permitiendo a los científicos y médicos hacer descubrimientos que podrían cambiar el rumbo de la ciencia y la salud. La interconexión entre estos conceptos no solo es un campo de estudio fascinante, sino que también tiene el potencial de impactar positivamente en la vida de las personas en todo el mundo.