La Ley de Henry y la Ley de Raoult son dos principios fundamentales en la química que se utilizan para describir el comportamiento de los gases y líquidos en soluciones. Ambas leyes son esenciales para entender cómo las sustancias se comportan en diferentes condiciones y son aplicadas en diversas áreas como la ingeniería química, la biología y la industria farmacéutica. Aunque estas leyes tratan sobre la solubilidad y la presión de vapor, respectivamente, tienen enfoques diferentes y se aplican en contextos distintos. En este artículo, exploraremos en profundidad estas dos leyes, sus diferencias, aplicaciones y ejemplos prácticos.
¿Qué es la Ley de Henry?
La Ley de Henry establece que la cantidad de gas disuelto en un líquido es proporcional a la presión parcial del gas sobre el líquido. Esta ley se puede expresar matemáticamente como: C = kH * P, donde C es la concentración del gas disuelto, kH es la constante de Henry y P es la presión parcial del gas. La constante de Henry varía para diferentes gases y líquidos, lo que significa que no todos los gases se comportan de la misma manera al disolverse en un líquido.
La Ley de Henry se aplica a soluciones diluidas y es especialmente relevante en situaciones donde los gases están en equilibrio con los líquidos. Por ejemplo, en la industria de las bebidas carbonatadas, el dióxido de carbono se disuelve en el líquido a alta presión, lo que permite que se mantenga en solución hasta que se abre la botella, liberando la presión y permitiendo que el gas escape.
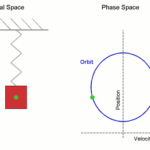 Diferencia entre movimiento armónico simple y movimiento periódico
Diferencia entre movimiento armónico simple y movimiento periódicoAplicaciones de la Ley de Henry
- Industria de bebidas: La Ley de Henry es fundamental en la producción de refrescos y cervezas, donde se requiere que el dióxido de carbono se disuelva en el líquido.
- Medicina: En la medicina, esta ley se aplica en la anestesia, donde los gases anestésicos deben ser solubles en la sangre para ser efectivos.
- Ecología: Se utiliza para entender cómo los gases como el oxígeno y el dióxido de carbono se disuelven en cuerpos de agua, lo que afecta la vida acuática.
¿Qué es la Ley de Raoult?
La Ley de Raoult se refiere a la presión de vapor de una solución y establece que la presión de vapor de un solvente en una solución es igual a la presión de vapor del solvente puro multiplicada por su fracción molar en la solución. Matemáticamente, se expresa como: Psolución = Xsolvente * Psolvente puro, donde Psolución es la presión de vapor de la solución, Xsolvente es la fracción molar del solvente y Psolvente puro es la presión de vapor del solvente puro.
La Ley de Raoult es especialmente importante en soluciones ideales, donde las interacciones entre las moléculas de soluto y solvente son similares a las interacciones entre las moléculas del solvente puro. Esta ley permite predecir cómo la adición de un soluto a un solvente afectará la presión de vapor del solvente. Por ejemplo, al añadir sal al agua, la presión de vapor del agua disminuirá, lo que es un fenómeno importante en la cocina y la química de soluciones.
Aplicaciones de la Ley de Raoult
- Cocina: La Ley de Raoult explica por qué el agua salada hierve a una temperatura más alta que el agua pura.
- Química industrial: Se utiliza para diseñar procesos de destilación y separación de compuestos químicos.
- Investigación: En laboratorios, esta ley ayuda a entender el comportamiento de soluciones y mezclas en experimentos.
Diferencias clave entre la Ley de Henry y la Ley de Raoult
A pesar de que ambas leyes tratan sobre la solubilidad y el comportamiento de los líquidos y gases, existen diferencias clave entre ellas. La Ley de Henry se centra en la solubilidad de los gases en líquidos bajo condiciones de presión, mientras que la Ley de Raoult se ocupa de la presión de vapor de soluciones y cómo se ve afectada por la presencia de solutos. Esta diferencia fundamental en el enfoque hace que cada ley sea útil en contextos distintos y para diferentes tipos de análisis.
 Diferencia entre el ácido sulfúrico y el ácido sulfónico
Diferencia entre el ácido sulfúrico y el ácido sulfónicoOtra diferencia significativa es que la Ley de Henry se aplica principalmente a soluciones diluidas de gases, mientras que la Ley de Raoult se aplica a soluciones de líquidos, especialmente en situaciones donde el soluto y el solvente son líquidos. Esto significa que la Ley de Raoult es más relevante para el estudio de soluciones líquidas, mientras que la Ley de Henry es crucial para entender la solubilidad de gases en líquidos.
Ejemplos prácticos de diferencias
- Ejemplo de la Ley de Henry: Si se coloca un gas como el oxígeno en un recipiente con agua, la cantidad de oxígeno disuelta dependerá de la presión parcial del oxígeno en el aire sobre el agua.
- Ejemplo de la Ley de Raoult: Si se mezcla etanol con agua, la presión de vapor de la mezcla dependerá de las fracciones molares de cada componente y de la presión de vapor del etanol puro.
Condiciones de validez de cada ley
Las condiciones bajo las cuales cada ley es válida son también un aspecto importante a considerar. La Ley de Henry es más precisa en condiciones de baja concentración de gas disuelto, donde el comportamiento del gas es ideal. A medida que la concentración de gas aumenta, las interacciones entre las moléculas de gas comienzan a afectar la solubilidad, y la ley puede no ser tan precisa. Por lo tanto, es crucial entender el contexto en el que se aplica esta ley para obtener resultados confiables.
Por otro lado, la Ley de Raoult es válida principalmente para soluciones ideales, donde las interacciones entre las moléculas del soluto y el solvente son similares a las interacciones entre las moléculas del solvente puro. En soluciones no ideales, donde hay interacciones significativas entre el soluto y el solvente, la ley puede no aplicarse de manera efectiva. En estos casos, se deben utilizar correcciones o modelos más complejos para predecir el comportamiento de la solución.
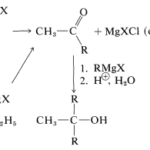 Diferencia entre el organolitio y el Grignard
Diferencia entre el organolitio y el GrignardFactores que afectan la validez de las leyes
- Temperatura: La temperatura puede afectar la solubilidad de los gases y la presión de vapor de los líquidos, lo que influye en la aplicabilidad de ambas leyes.
- Concentración: La concentración del soluto o gas en la solución es un factor determinante en la validez de ambas leyes.
- Interacciones moleculares: La naturaleza de las interacciones entre las moléculas de soluto y solvente puede hacer que una de las leyes sea más aplicable que la otra.
Implicaciones en la vida diaria
Las implicaciones de la Ley de Henry y la Ley de Raoult en la vida diaria son numerosas y variadas. Desde la forma en que consumimos bebidas carbonatadas hasta la manera en que cocinamos o preparamos soluciones químicas, ambas leyes están presentes en nuestras actividades cotidianas. Por ejemplo, cuando abrimos una botella de refresco, la liberación de gas que escuchamos es el resultado de la disminución de presión, lo que permite que el dióxido de carbono escape. Esto es un claro ejemplo de la Ley de Henry en acción.
En la cocina, al preparar una pasta en agua con sal, la Ley de Raoult se manifiesta al elevar la temperatura de ebullición del agua. Esto es especialmente útil para los chefs que buscan optimizar sus procesos de cocción. La comprensión de estas leyes también es vital para los científicos que trabajan en el desarrollo de nuevos medicamentos, donde la solubilidad de los gases y líquidos puede influir en la eficacia de un fármaco.
Ejemplos cotidianos
- Bebidas gaseosas: El dióxido de carbono se disuelve en la bebida bajo presión, siguiendo la Ley de Henry.
- Agua salada: La sal en el agua afecta la temperatura de ebullición, un fenómeno explicado por la Ley de Raoult.
- Medicamentos: La solubilidad de un gas anestésico en la sangre se puede entender mejor a través de la Ley de Henry.
Conclusiones sobre la Ley de Henry y la Ley de Raoult
tanto la Ley de Henry como la Ley de Raoult son fundamentales para entender cómo los gases y líquidos interactúan en diferentes condiciones. Aunque se aplican en contextos diferentes y tienen enfoques distintos, ambas leyes son cruciales para diversas aplicaciones en la ciencia y la industria. La comprensión de estas leyes no solo es importante para los científicos, sino que también tiene implicaciones prácticas en nuestra vida diaria, desde la forma en que disfrutamos de nuestras bebidas hasta cómo cocinamos y preparamos soluciones químicas.
El estudio de estas leyes nos permite apreciar mejor el mundo que nos rodea y cómo las propiedades de los materiales afectan nuestra vida cotidiana. Al comprender la diferencia entre la Ley de Henry y la Ley de Raoult, podemos tener una base sólida para explorar más a fondo la química y sus aplicaciones en el mundo real.
