Los espectros atómicos y los espectros moleculares son dos conceptos fundamentales en la química y la física que nos ayudan a entender cómo interactúan la luz y la materia. A pesar de que ambos tipos de espectros son herramientas valiosas para el análisis de la composición y estructura de la materia, existen diferencias significativas entre ellos. Estas diferencias se deben a la naturaleza de los átomos y las moléculas, así como a las transiciones electrónicas que ocurren en cada caso. A continuación, exploraremos en detalle estas diferencias y cómo se manifiestan en la práctica.
Definición de espectros atómicos
Los espectros atómicos son el resultado de las transiciones electrónicas que ocurren en los átomos individuales. Cuando un átomo absorbe o emite luz, los electrones dentro de ese átomo pueden saltar de un nivel de energía a otro. Este proceso se traduce en la emisión o absorción de fotones a longitudes de onda específicas. Cada elemento químico tiene un conjunto único de niveles de energía, lo que significa que su espectro atómico también será único. Esta característica permite a los científicos identificar la composición de una muestra a partir de su espectro atómico.
 Diferencia entre polímero lineal y reticulado
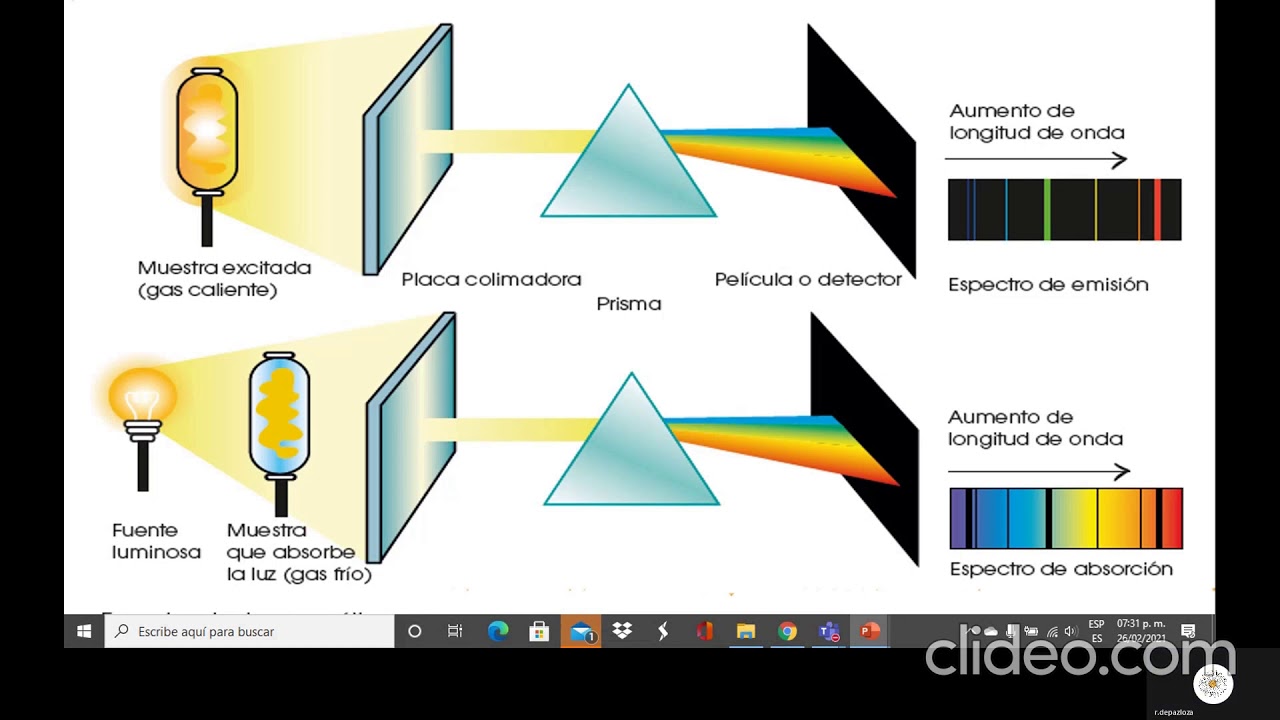
Diferencia entre polímero lineal y reticuladoLos espectros atómicos pueden clasificarse en dos categorías principales: espectros de absorción y espectros de emisión. En el caso de los espectros de absorción, un átomo absorbe luz de ciertas longitudes de onda, lo que provoca que aparezcan líneas oscuras en el espectro. Por otro lado, en los espectros de emisión, los átomos emiten luz en longitudes de onda específicas, lo que resulta en líneas brillantes. Estas líneas se conocen como líneas espectrales y son la clave para identificar elementos en una muestra.
Definición de espectros moleculares
Los espectros moleculares se generan a partir de moléculas, que son grupos de átomos unidos por enlaces químicos. A diferencia de los átomos individuales, las moléculas tienen estructuras más complejas y, por lo tanto, sus espectros son más complicados. Las transiciones electrónicas en las moléculas no solo involucran cambios en los niveles de energía de los electrones, sino que también incluyen cambios en la vibración y la rotación de los enlaces entre átomos. Esto da como resultado un espectro que no solo muestra líneas espectrales, sino también bandas más amplias que representan diferentes modos de vibración y rotación.
Al igual que los espectros atómicos, los espectros moleculares también pueden ser de absorción o emisión. Sin embargo, en el caso de los espectros moleculares, las bandas de absorción suelen ser más anchas debido a la variedad de transiciones posibles. Las moléculas pueden vibrar y rotar en diferentes modos, lo que resulta en una mayor complejidad en su espectro. Esto hace que los espectros moleculares sean herramientas poderosas para estudiar la estructura y las interacciones de las moléculas.
 Diferencia entre Tris Base y Tris HCl
Diferencia entre Tris Base y Tris HClDiferencias clave entre espectros atómicos y moleculares
Una de las diferencias más significativas entre los espectros atómicos y los espectros moleculares radica en la complejidad de los espectros. Los espectros atómicos suelen ser más simples y consisten en líneas discretas, mientras que los espectros moleculares son más complejos y se presentan en forma de bandas. Esta complejidad se debe a las múltiples transiciones electrónicas, vibracionales y rotacionales que pueden ocurrir en las moléculas.
Otra diferencia importante es la resolución espectral. Los espectros atómicos, al estar compuestos por líneas discretas, suelen tener una resolución espectral más alta, lo que permite una identificación más precisa de los elementos. En contraste, los espectros moleculares, debido a la superposición de múltiples bandas, pueden tener una resolución espectral más baja, lo que puede dificultar la identificación de las moléculas presentes en una muestra.
Comparación de las transiciones electrónicas
- Transiciones electrónicas en átomos: En los átomos, las transiciones se producen entre niveles de energía bien definidos, lo que resulta en líneas espectrales bien separadas.
- Transiciones electrónicas en moléculas: En las moléculas, las transiciones pueden involucrar cambios en los niveles de energía, así como en los modos de vibración y rotación, lo que da lugar a bandas espectrales más anchas.
La diferencia en la naturaleza de las transiciones electrónicas también influye en la forma en que se interpretan los espectros. Los espectros atómicos son más fáciles de analizar debido a su simplicidad, mientras que los espectros moleculares requieren un análisis más detallado para comprender las diferentes contribuciones de las transiciones vibracionales y rotacionales.
 Diferencia entre los espectros de emisión de hidrógeno y helio
Diferencia entre los espectros de emisión de hidrógeno y helioAplicaciones de los espectros atómicos
Los espectros atómicos tienen numerosas aplicaciones en diversas áreas de la ciencia. Una de las aplicaciones más comunes es en la espectroscopia de absorción atómica, que se utiliza para determinar la concentración de elementos en una muestra. Esta técnica es especialmente útil en el análisis de metales pesados en el agua y en suelos, así como en la industria alimentaria para garantizar la seguridad de los productos.
Otra aplicación importante de los espectros atómicos es en la espectroscopia de emisión atómica, que se utiliza en la identificación de elementos en muestras de materiales como minerales y metales. Esta técnica permite a los científicos analizar la composición de una muestra de manera rápida y precisa, lo que es esencial en la investigación y el desarrollo de nuevos materiales.
Aplicaciones de los espectros moleculares
Los espectros moleculares también tienen una amplia gama de aplicaciones en la ciencia y la tecnología. Una de las aplicaciones más importantes es en la espectroscopia infrarroja, que se utiliza para identificar compuestos orgánicos y funcionales. Esta técnica se basa en la absorción de luz infrarroja por las moléculas, lo que provoca cambios en sus modos de vibración. Los espectros obtenidos permiten a los científicos identificar grupos funcionales y estructuras moleculares.
Otra aplicación relevante de los espectros moleculares es en la espectroscopia de resonancia magnética nuclear (RMN), que se utiliza para determinar la estructura de compuestos orgánicos complejos. La RMN proporciona información detallada sobre el entorno químico de los núcleos atómicos en una molécula, lo que permite a los científicos deducir la estructura tridimensional de las moléculas.
Conclusiones sobre las diferencias entre espectros atómicos y moleculares
En resumen, los espectros atómicos y los espectros moleculares son herramientas esenciales en el análisis químico y físico. A pesar de que ambos tipos de espectros se utilizan para estudiar la interacción de la luz con la materia, sus diferencias en complejidad, resolución y aplicaciones los hacen únicos. Los espectros atómicos son ideales para la identificación de elementos individuales, mientras que los espectros moleculares son más adecuados para el análisis de compuestos complejos. Ambas técnicas son fundamentales para el avance de la ciencia y la tecnología en múltiples campos.