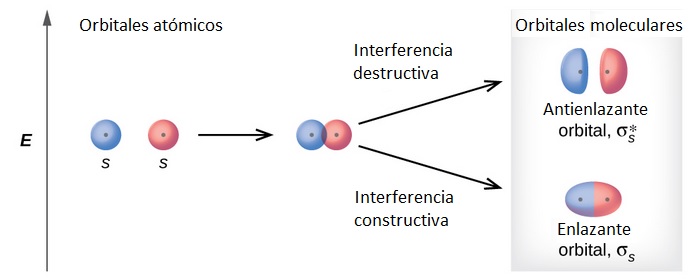
La química molecular es una rama fascinante de la ciencia que se ocupa de las interacciones entre átomos y moléculas. Uno de los conceptos fundamentales en este campo es la teoría de orbitales moleculares. Esta teoría ayuda a explicar cómo se forman los enlaces entre los átomos y cómo se distribuyen los electrones en las moléculas. En este contexto, es crucial entender la diferencia entre orbitales moleculares enlazantes y orbitales moleculares antienlazantes. Estos dos tipos de orbitales tienen propiedades y funciones diferentes que afectan la estabilidad y la reactividad de las moléculas.
Orbitales Moleculares Enlazantes
Los orbitales moleculares enlazantes son aquellos que se forman cuando dos orbitales atómicos se combinan de manera constructiva. Esta combinación resulta en un orbital que tiene una menor energía que los orbitales atómicos originales, lo que favorece la formación de enlaces. Cuando los electrones ocupan estos orbitales, se produce una atracción entre los núcleos de los átomos involucrados, lo que contribuye a la estabilidad de la molécula. En términos simples, estos orbitales ayudan a mantener unidos a los átomos en una molécula.
Una de las características más importantes de los orbitales moleculares enlazantes es que tienen una alta densidad electrónica entre los núcleos de los átomos. Esto significa que los electrones se encuentran en la región del espacio donde se produce la atracción entre los núcleos, lo que refuerza el enlace. Un ejemplo común de un orbital molecular enlazante es el orbital sigma (σ), que se forma por la superposición frontal de dos orbitales atómicos. Este tipo de orbital es fundamental en la formación de enlaces simples entre átomos.
 Centro estereogénico vs. centro quiral
Centro estereogénico vs. centro quiralAdemás de los orbitales sigma, también existen los orbitales pi (π), que se forman cuando dos orbitales atómicos se superponen lateralmente. Estos orbitales son típicos en enlaces dobles y triples. Aunque los orbitales pi son menos fuertes que los orbitales sigma, su presencia es crucial para la geometría y la reactividad de muchas moléculas. En resumen, los orbitales moleculares enlazantes son esenciales para entender cómo se mantienen unidas las moléculas y cómo se comportan en diferentes condiciones.
Orbitales Moleculares Antienlazantes
Por otro lado, los orbitales moleculares antienlazantes se forman cuando dos orbitales atómicos se combinan de manera destructiva. En este caso, la combinación resulta en un orbital que tiene una energía mayor que la de los orbitales atómicos originales. Cuando los electrones ocupan estos orbitales, se produce una repulsión entre los núcleos de los átomos, lo que puede llevar a una disminución en la estabilidad de la molécula. En otras palabras, los orbitales antienlazantes tienden a debilitar los enlaces entre los átomos.
Una característica distintiva de los orbitales antienlazantes es que tienen una región de nodos, donde la densidad electrónica es cero. Esto significa que en la región donde se espera que haya una atracción entre los núcleos, en realidad hay una repulsión, lo que dificulta la formación de un enlace fuerte. Un ejemplo de un orbital antienlazante es el orbital sigma antienlazante (σ*), que se forma cuando los orbitales atómicos se superponen de tal manera que sus fases se cancelan. Este tipo de orbital es crucial para entender la inestabilidad de ciertos compuestos.
 Diferencia entre alcanos y alquenos
Diferencia entre alcanos y alquenosLos orbitales antienlazantes también incluyen orbitales pi antienlazantes (π*), que se forman de manera similar a los orbitales pi enlazantes, pero con la diferencia de que su combinación resulta en una mayor energía. La ocupación de estos orbitales puede ser un indicativo de que una molécula es reactiva o inestable. En resumen, los orbitales moleculares antienlazantes son fundamentales para comprender la reactividad de las moléculas y cómo pueden descomponerse o reaccionar con otras sustancias.
Diferencias Clave entre Orbitales Enlazantes y Antienlazantes
Existen varias diferencias clave entre los orbitales moleculares enlazantes y antienlazantes que son importantes para entender su función en la química. En primer lugar, la energía de estos orbitales es un aspecto fundamental. Los orbitales enlazantes tienen una energía más baja que los orbitales atómicos originales, lo que favorece la formación de enlaces estables. En contraste, los orbitales antienlazantes tienen una energía más alta, lo que tiende a debilitar los enlaces.
- Energía: Los orbitales enlazantes son de menor energía; los antienlazantes son de mayor energía.
- Densidad Electrónica: Los orbitales enlazantes tienen alta densidad electrónica entre los núcleos; los antienlazantes tienen nodos donde la densidad es cero.
- Estabilidad: Los orbitales enlazantes contribuyen a la estabilidad de la molécula; los antienlazantes la disminuyen.
- Tipos de Enlace: Los orbitales enlazantes forman enlaces estables; los antienlazantes pueden indicar reactividad.
Otra diferencia importante es la distribución de electrones. En los orbitales enlazantes, los electrones se encuentran en regiones que favorecen la atracción entre los núcleos. Por el contrario, en los orbitales antienlazantes, la distribución de electrones se encuentra en regiones que tienden a alejar a los núcleos, lo que resulta en una repulsión. Esta diferencia en la distribución de electrones es crucial para entender cómo se comportan las moléculas en reacciones químicas y en su estabilidad general.
 Diferencia entre el efecto Tyndall y el movimiento browniano
Diferencia entre el efecto Tyndall y el movimiento brownianoPor último, la ocupación de estos orbitales también tiene implicaciones significativas. En una molécula estable, los orbitales enlazantes están llenos de electrones, mientras que los orbitales antienlazantes tienden a estar vacíos o parcialmente ocupados. La presencia de electrones en los orbitales antienlazantes puede indicar una posible reacción o descomposición de la molécula. Esta ocupación es un aspecto clave en la predicción de la reactividad química y la estabilidad de las sustancias.
Ejemplos Prácticos
Para ilustrar la diferencia entre orbitales moleculares enlazantes y antienlazantes, consideremos el caso del molecular diatómico más simple: el hidrógeno (H2). En este caso, cada átomo de hidrógeno tiene un único electrón que se combina para formar un enlace. Cuando los orbitales atómicos de los dos átomos de hidrógeno se combinan, se forma un orbital enlazante (σ) que contiene dos electrones. Este orbital es responsable de la estabilidad de la molécula de H2.
Sin embargo, si consideramos un sistema donde se introducen electrones adicionales, como en el caso del ion hidrógeno positivo (H2+), la situación cambia. En este caso, el sistema puede tener un orbital antienlazante (σ*) vacío, lo que indica que la estabilidad del ion es menor que la del H2. La presencia de un orbital antienlazante vacío sugiere que el ion es menos estable y puede reaccionar con otras especies químicas para formar nuevos compuestos.
Otro ejemplo es el caso del oxígeno (O2). En esta molécula, se forman orbitales enlazantes y antienlazantes. Los orbitales enlazantes son responsables de la formación de un enlace fuerte entre los dos átomos de oxígeno, mientras que los orbitales antienlazantes contienen electrones que pueden influir en la reactividad del oxígeno. La ocupación de estos orbitales es un factor clave que explica por qué el oxígeno es un agente oxidante y participa en numerosas reacciones químicas.
Aplicaciones en la Química
La comprensión de los orbitales moleculares enlazantes y antienlazantes tiene aplicaciones prácticas en diversos campos de la química. Por ejemplo, en la química orgánica, la teoría de orbitales moleculares se utiliza para predecir la reactividad de diferentes compuestos. Al analizar la ocupación de orbitales en una molécula, los químicos pueden anticipar cómo reaccionará esa molécula en presencia de otros reactivos.
En la química inorgánica, la teoría de orbitales moleculares también juega un papel fundamental en la comprensión de la estructura y propiedades de complejos metálicos. Estos complejos pueden tener orbitales antienlazantes que afectan su estabilidad y reactividad. Por lo tanto, al estudiar estos orbitales, los químicos pueden diseñar nuevos materiales con propiedades específicas, como catalizadores o materiales semiconductores.
Asimismo, en la bioquímica, la teoría de orbitales moleculares se aplica en la comprensión de las interacciones entre biomoléculas, como enzimas y sustratos. Al entender cómo se forman los enlaces y cómo se distribuyen los electrones en estos sistemas, los investigadores pueden desarrollar nuevos fármacos o terapias para tratar enfermedades. En resumen, la teoría de orbitales moleculares tiene un impacto significativo en diversas disciplinas científicas.
Conclusiones sobre la Teoría de Orbitales Moleculares
La teoría de orbitales moleculares, que incluye tanto los orbitales enlazantes como los antienlazantes, es esencial para comprender cómo se forman los enlaces y cómo se comportan las moléculas en diferentes condiciones. Los orbitales enlazantes son fundamentales para la estabilidad de las moléculas, mientras que los orbitales antienlazantes indican áreas de posible reactividad. Al estudiar estos conceptos, los químicos pueden predecir la reactividad y las propiedades de las sustancias, lo que es crucial para el avance de la ciencia y la tecnología.
La diferenciación entre estos dos tipos de orbitales no solo es un ejercicio académico, sino que tiene aplicaciones prácticas en la investigación y desarrollo de nuevos materiales, medicamentos y procesos químicos. A medida que la ciencia avanza, la comprensión de los orbitales moleculares seguirá siendo un pilar fundamental en el estudio de la química y sus aplicaciones en el mundo real.