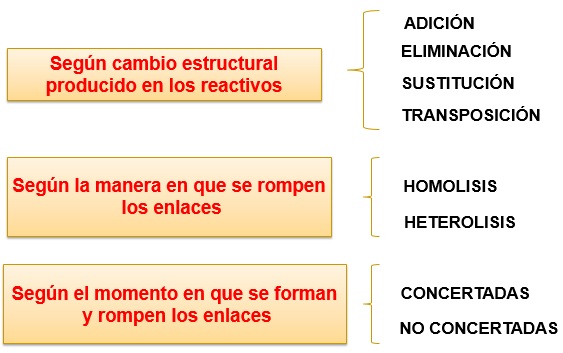
Las reacciones químicas son procesos fundamentales en la química que permiten la transformación de sustancias. Entre estas reacciones, dos de las más importantes son las reacciones de adición y las reacciones de sustitución. Aunque ambas son esenciales en la formación de compuestos químicos, tienen características y mecanismos diferentes. En este artículo, exploraremos en detalle estas diferencias, proporcionando ejemplos y aplicaciones para una mejor comprensión.
Reacciones de adición
Las reacciones de adición son aquellas en las que dos o más reactivos se combinan para formar un solo producto. Este tipo de reacción es común en compuestos insaturados, como los alquenos y alquinos, que contienen dobles o triples enlaces. Durante una reacción de adición, se rompe un enlace múltiple y se forman nuevos enlaces simples, lo que resulta en un aumento en el número de átomos en el producto final. Este proceso puede ser observado en diversas reacciones, como la hidratación de etileno.
Un ejemplo clásico de una reacción de adición es la hidrogenación de un alqueno. En este proceso, el etileno (C2H4) reacciona con hidrógeno (H2) en presencia de un catalizador, como el níquel, para formar etano (C2H6). La reacción puede representarse de la siguiente manera:
 ¿Cuáles son algunas excepciones a los postulados de Koch?
¿Cuáles son algunas excepciones a los postulados de Koch?- C2H4 + H2 → C2H6
Este tipo de reacción es de gran importancia en la industria química, ya que permite la producción de compuestos saturados a partir de insaturados, lo que puede ser útil en la fabricación de plásticos, combustibles y otros productos químicos. Además, las reacciones de adición pueden ser de diferentes tipos, como la adición de halógenos, donde los halógenos se añaden a un alqueno, formando dihaluros.
Reacciones de sustitución
Por otro lado, las reacciones de sustitución implican el reemplazo de un átomo o grupo de átomos en un compuesto por otro. Este tipo de reacción puede clasificarse en dos categorías principales: sustitución nucleofílica y sustitución electrófila. En la sustitución nucleofílica, un nucleófilo (una especie que dona un par de electrones) ataca un carbono, desplazando un grupo saliente. Por ejemplo, en la reacción entre un halogenuro de alquilo y un nucleófilo, el nucleófilo sustituye al halógeno.
Un ejemplo típico de reacción de sustitución es la reacción entre el cloruro de metilo (CH3Cl) y el ion hidróxido (OH-). En esta reacción, el ion hidróxido actúa como nucleófilo y sustituye al cloro, formando metanol (CH3OH):
 Diferencia entre anemia y hemofilia
Diferencia entre anemia y hemofilia- CH3Cl + OH- → CH3OH + Cl-
Las reacciones de sustitución son muy comunes en la química orgánica y se utilizan en la síntesis de una variedad de compuestos. Son esenciales en la producción de fármacos, agroquímicos y otros productos químicos de interés. Además, estas reacciones pueden ser influenciadas por varios factores, como la estructura del sustrato, la naturaleza del nucleófilo y las condiciones de reacción.
Diferencias clave entre reacciones de adición y sustitución
Una de las diferencias más notables entre las reacciones de adición y sustitución es el número de productos formados. En una reacción de adición, generalmente se forma un único producto a partir de varios reactivos, mientras que en una reacción de sustitución, se generan al menos dos productos: el nuevo compuesto y el grupo que ha sido desplazado. Esto es fundamental para entender cómo estas reacciones se utilizan en la química y la industria.
Otra diferencia importante es el tipo de enlaces que se forman y se rompen. En las reacciones de adición, se rompen enlaces múltiples (dobles o triples) para formar enlaces simples, mientras que en las reacciones de sustitución, un enlace simple se rompe y se forma otro enlace simple en su lugar. Esta distinción es crucial porque afecta la energía de activación y la velocidad de la reacción.
 Diferencia entre el abeto y el pino
Diferencia entre el abeto y el pinoEjemplos prácticos de reacciones de adición
Las reacciones de adición tienen múltiples aplicaciones en la industria. Un ejemplo práctico es la producción de polímeros a partir de monómeros insaturados. Los monómeros, como el etileno, se someten a reacciones de adición para formar largas cadenas de polímeros. Este proceso se conoce como polimerización por adición y es fundamental en la fabricación de plásticos como el polietileno y el polipropileno.
Otro ejemplo se encuentra en la industria alimentaria, donde la hidrogenación de aceites se utiliza para convertir aceites insaturados en grasas saturadas. Este proceso no solo mejora la estabilidad y la vida útil de los productos, sino que también afecta su textura y sabor. Sin embargo, el uso excesivo de grasas saturadas puede tener implicaciones para la salud, lo que ha llevado a un mayor interés en aceites no hidrogenados y alternativas más saludables.
Ejemplos prácticos de reacciones de sustitución
Las reacciones de sustitución también son ampliamente utilizadas en la industria química. Un ejemplo es la síntesis de fármacos. Muchas veces, se requiere modificar la estructura de un compuesto base para mejorar su actividad biológica. A través de reacciones de sustitución, se pueden introducir grupos funcionales que alteran las propiedades del fármaco, lo que resulta en compuestos más eficaces o con menos efectos secundarios.
Otro ejemplo se puede observar en la producción de detergentes. La reacción de sustitución se utiliza para crear surfactantes que son efectivos en la eliminación de grasas y suciedad. Los grupos funcionales se sustituyen en moléculas para mejorar su capacidad de interacción con el agua y el aceite, lo que resulta en productos de limpieza más eficientes.
Factores que influyen en las reacciones de adición y sustitución
Varios factores pueden influir en la velocidad y el resultado de las reacciones de adición y sustitución. En el caso de las reacciones de adición, la presencia de un catalizador puede acelerar el proceso. Por ejemplo, en la hidrogenación de alquenos, el uso de un catalizador como el níquel o el paladio puede facilitar la reacción, permitiendo que se lleve a cabo a temperaturas y presiones más bajas.
En las reacciones de sustitución, la estructura del sustrato es un factor clave. Los compuestos primarios, secundarios y terciarios tienen diferentes reactividades en estas reacciones. Por ejemplo, los halogenuros de alquilo terciarios tienden a reaccionar más rápidamente en reacciones de sustitución nucleofílica debido a la estabilidad del carbocatión que se forma durante el proceso. Además, la naturaleza del nucleófilo y las condiciones de reacción, como la temperatura y el solvente, también juegan un papel importante en la eficacia de la reacción.
Comparación de mecanismos
Los mecanismos de reacción son fundamentales para entender cómo ocurren las reacciones de adición y sustitución. En las reacciones de adición, el mecanismo suele implicar la formación de un intermediario. Por ejemplo, en la adición de bromuro de hidrógeno a un alqueno, se forma un ion bromonio como intermediario, lo que facilita la adición del nucleófilo. Este mecanismo puede ser considerado como un proceso de dos etapas, donde primero se forma el intermediario y luego se completa la reacción con la adición del nucleófilo.
Por otro lado, las reacciones de sustitución pueden seguir mecanismos diferentes, dependiendo del tipo de reacción. En la sustitución nucleofílica, el mecanismo puede ser bimolecular (SN2), donde el nucleófilo y el sustrato reaccionan simultáneamente, o unimolecular (SN1), donde se forma un carbocatión como intermediario. Este último mecanismo es más común en compuestos terciarios, donde el carbocatión es más estable. Comprender estos mecanismos es esencial para predecir el resultado de las reacciones y su velocidad.
Aplicaciones en la vida cotidiana
Las reacciones de adición y sustitución tienen aplicaciones en nuestra vida diaria que a menudo pasan desapercibidas. Por ejemplo, los cosméticos que usamos a diario a menudo contienen compuestos que se producen a través de reacciones de sustitución. La modificación de moléculas para crear fragancias o emolientes es un proceso común en la industria de la belleza. Los ingredientes activos que se añaden a las cremas y lociones son a menudo el resultado de reacciones químicas que mejoran la eficacia de los productos.
Asimismo, las reacciones de adición son fundamentales en la producción de alimentos procesados. La hidrogenación de aceites para crear margarina es un ejemplo claro de cómo las reacciones químicas afectan la industria alimentaria. La química detrás de estos procesos determina no solo la textura y el sabor, sino también las propiedades nutricionales de los productos que consumimos.
Consideraciones ambientales
Es importante considerar el impacto ambiental de las reacciones químicas, tanto de adición como de sustitución. Por ejemplo, la producción de plásticos a través de reacciones de adición ha llevado a un aumento significativo en los residuos plásticos en el medio ambiente. La acumulación de estos materiales ha generado preocupación sobre su descomposición y los efectos en la fauna y flora. Por ello, la investigación se ha centrado en desarrollar métodos más sostenibles para la producción de plásticos, buscando alternativas biodegradables.
En el caso de las reacciones de sustitución, la síntesis de fármacos y otros compuestos químicos también plantea desafíos ambientales. Los productos químicos utilizados en estas reacciones pueden ser tóxicos y generar residuos peligrosos. La industria química está trabajando para minimizar estos efectos, buscando métodos más limpios y eficientes que reduzcan el impacto ambiental de sus procesos.
Futuras tendencias en la investigación
El estudio de las reacciones de adición y sustitución sigue siendo un área activa de investigación en la química. Se están explorando nuevos catalizadores que pueden mejorar la eficiencia de estas reacciones, así como métodos más sostenibles para llevar a cabo procesos químicos. La química verde, que se centra en la reducción de desechos y el uso de recursos renovables, es un enfoque que está ganando terreno en la investigación química.
Además, la biocatálisis, que utiliza enzimas para facilitar reacciones químicas, está emergiendo como una alternativa prometedora. Estas enzimas pueden llevar a cabo reacciones de adición y sustitución de manera más eficiente y con menos impacto ambiental, lo que podría transformar la forma en que producimos compuestos químicos en el futuro.
Resumiendo las diferencias
las reacciones de adición y sustitución son dos tipos fundamentales de reacciones químicas que tienen características y aplicaciones distintas. Las reacciones de adición implican la combinación de reactivos para formar un único producto, mientras que las reacciones de sustitución implican el reemplazo de un átomo o grupo de átomos por otro. Ambas son esenciales en la química orgánica y tienen un impacto significativo en la industria y en nuestra vida cotidiana.
Comprender estas diferencias no solo es crucial para los estudiantes de química, sino también para cualquier persona interesada en cómo funcionan los procesos químicos en el mundo que nos rodea. Desde la producción de plásticos y fármacos hasta las reacciones que ocurren en nuestros cuerpos, las reacciones de adición y sustitución son componentes clave en la química y en la vida diaria.