Las reacciones químicas son procesos fundamentales en la ciencia, y su comprensión es crucial para muchas disciplinas, desde la química hasta la biología. Uno de los aspectos más importantes de estas reacciones es su velocidad, que puede variar significativamente. En este artículo, exploraremos la diferencia entre reacciones de primer y segundo orden. Estas diferencias se basan en cómo la velocidad de la reacción depende de las concentraciones de los reactivos involucrados.
Reacciones de Primer Orden
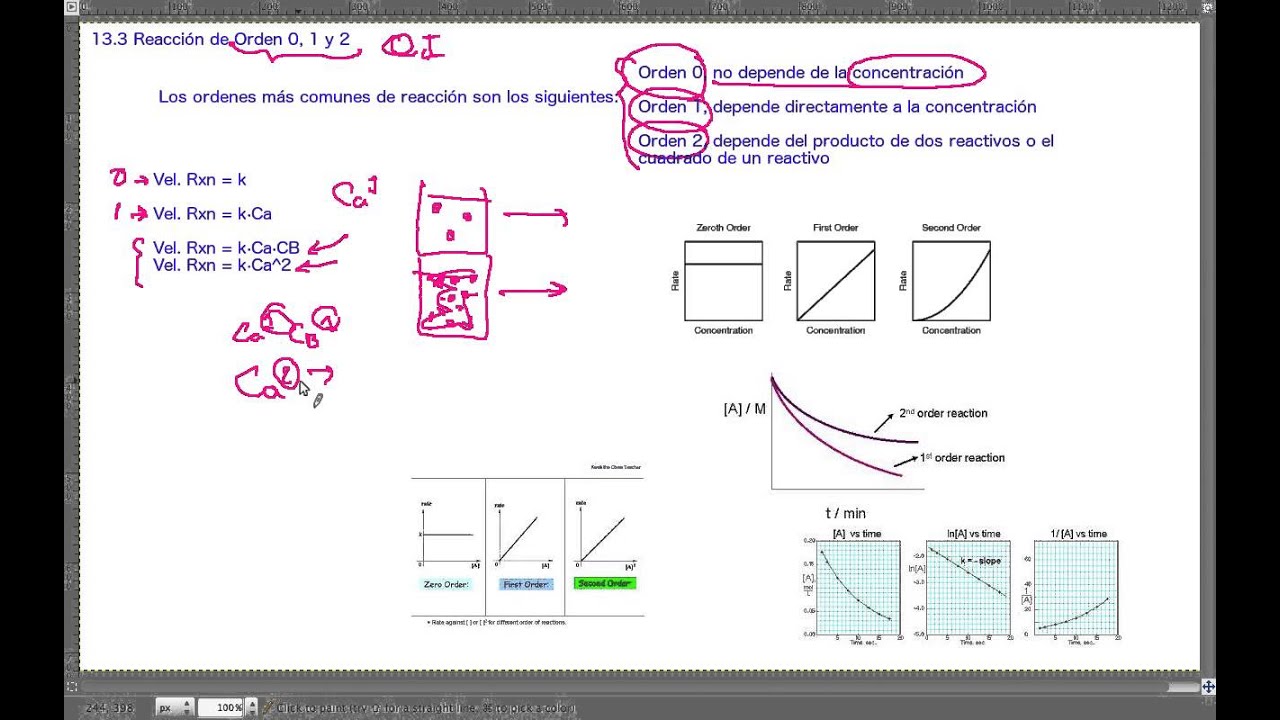
Las reacciones de primer orden son aquellas en las que la velocidad de la reacción es directamente proporcional a la concentración de uno de los reactivos. Esto significa que si duplicamos la concentración de ese reactivo, la velocidad de la reacción también se duplicará. Este tipo de reacción se puede representar matemáticamente con la ecuación: v = k[A], donde v es la velocidad de la reacción, k es la constante de velocidad y [A] es la concentración del reactivo.
 Diferencia entre epidermis e hipodermis
Diferencia entre epidermis e hipodermisUn ejemplo clásico de una reacción de primer orden es la descomposición del peróxido de hidrógeno (H₂O₂) en agua y oxígeno. La velocidad de esta reacción depende únicamente de la concentración de peróxido de hidrógeno. A medida que se va consumiendo el H₂O₂, la velocidad de producción de oxígeno disminuye, reflejando la disminución de la concentración del reactivo.
Las reacciones de primer orden son comunes en procesos biológicos y químicos. Por ejemplo, muchos procesos de metabolismo celular siguen cinéticas de primer orden. Esto es importante en el diseño de fármacos, donde la eliminación de un medicamento del cuerpo puede ser modelada como una reacción de primer orden, lo que facilita la predicción de su comportamiento en el organismo.
Características de las Reacciones de Primer Orden
- Proporcionalidad: La velocidad de la reacción es proporcional a la concentración del reactivo.
- Constante de Velocidad: La constante de velocidad k es específica para cada reacción y depende de factores como la temperatura.
- Gráficos: Un gráfico de la concentración del reactivo contra el tiempo mostrará una curva exponencial decreciente.
- Medición: La determinación de la constante de velocidad se puede realizar mediante métodos experimentales como la técnica de integración.
Reacciones de Segundo Orden
Las reacciones de segundo orden son más complejas, ya que su velocidad depende de las concentraciones de dos reactivos o del cuadrado de la concentración de uno solo. La ecuación general para una reacción de segundo orden puede expresarse como: v = k[A][B] o v = k[A]2, dependiendo de cómo se desarrollen. En este caso, si la concentración de cualquiera de los reactivos se duplica, la velocidad de la reacción se cuadruplica.
 Diferencia entre ganso y pato
Diferencia entre ganso y patoUn ejemplo típico de una reacción de segundo orden es la reacción entre el oxígeno y el ozono, donde ambos reactivos están involucrados. A medida que se incrementa la concentración de cualquiera de los dos, la velocidad de la reacción aumenta de manera significativa, lo que hace que estas reacciones sean más rápidas en comparación con las de primer orden.
Las reacciones de segundo orden son comunes en reacciones de acido-base y en ciertas reacciones de oxidación. Estas reacciones son importantes en el estudio de la cinética química, ya que su comportamiento puede ser más complicado y, a menudo, requiere un análisis más profundo para entender cómo las condiciones afectan la velocidad de reacción.
Características de las Reacciones de Segundo Orden
- Dependencia de Concentración: La velocidad depende de las concentraciones de dos reactivos o del cuadrado de uno solo.
- Constante de Velocidad: La constante de velocidad k puede variar con la temperatura y la naturaleza de los reactivos.
- Gráficos: Un gráfico de la concentración de uno de los reactivos contra el tiempo mostrará una curva que se aplana a medida que la reacción avanza.
- Reacciones Rápidas: Suelen ser más rápidas que las reacciones de primer orden debido a la mayor dependencia de la concentración.
Diferencias Clave entre Reacciones de Primer y Segundo Orden
Una de las diferencias más evidentes entre las reacciones de primer y segundo orden es la relación entre la velocidad de reacción y la concentración de los reactivos. En las reacciones de primer orden, la velocidad es directamente proporcional a la concentración de un solo reactivo, mientras que en las reacciones de segundo orden, la velocidad puede depender de dos reactivos o del cuadrado de uno solo. Esta diferencia en la dependencia de la concentración tiene un impacto significativo en cómo se desarrollan y se estudian estas reacciones.
 Diferencia entre la goma y el mucílago
Diferencia entre la goma y el mucílagoOtra diferencia importante es el comportamiento cinético de las reacciones. Las reacciones de primer orden suelen mostrar un comportamiento exponencial en sus gráficos, mientras que las reacciones de segundo orden pueden mostrar un comportamiento más complejo. Esto se debe a que las reacciones de segundo orden pueden involucrar interacciones más complicadas entre los reactivos, lo que hace que su análisis cinético sea más desafiante.
Además, las reacciones de segundo orden tienden a tener una vida media que varía con la concentración del reactivo, a diferencia de las reacciones de primer orden, donde la vida media es constante. Esto significa que en una reacción de segundo orden, a medida que se consume el reactivo, el tiempo necesario para que se alcance la mitad de la concentración inicial cambia, lo que puede complicar la predicción de la duración de la reacción.
Comparación Resumida
- Orden: Primer orden depende de un reactivo; segundo orden depende de dos o del cuadrado de uno.
- Velocidad: Primer orden tiene velocidad proporcional a la concentración; segundo orden tiene velocidad proporcional al producto de las concentraciones.
- Gráficos: Primer orden muestra curva exponencial; segundo orden muestra un comportamiento más complejo.
- Vida Media: Constante en primer orden; variable en segundo orden.
Ejemplos Prácticos de Reacciones de Primer y Segundo Orden
Para ilustrar mejor las diferencias entre reacciones de primer y segundo orden, es útil considerar ejemplos prácticos. En el caso de una reacción de primer orden, tomemos el ejemplo de la descomposición del yodo en una reacción donde el yodo se descompone en productos a medida que se calienta. La velocidad de esta reacción se puede medir y se puede observar que es directamente proporcional a la concentración de yodo presente en el sistema.
Por otro lado, un ejemplo de reacción de segundo orden podría ser la reacción entre el ácido acético y el etanol para formar acetato de etilo. En esta reacción, la velocidad depende tanto de la concentración del ácido acético como de la concentración del etanol. Si aumentamos la concentración de cualquiera de los dos reactivos, la velocidad de la reacción aumentará de manera más pronunciada, lo que demuestra la naturaleza de segundo orden de esta reacción.
Estos ejemplos no solo ayudan a entender la diferencia entre los tipos de reacciones, sino que también ilustran cómo estas reacciones son relevantes en contextos industriales y biológicos. En la industria química, por ejemplo, la comprensión de estas cinéticas es crucial para optimizar procesos y aumentar la eficiencia en la producción de sustancias químicas.
Aplicaciones en la Vida Real
- Industria Química: Las reacciones de primer y segundo orden se aplican en la producción de productos químicos, donde es necesario controlar la velocidad de reacción.
- Medicina: La cinética de primer orden se utiliza para modelar la eliminación de fármacos del cuerpo, ayudando a determinar dosis efectivas.
- Biología: Muchas reacciones metabólicas siguen patrones de primer y segundo orden, afectando cómo los organismos procesan nutrientes.
- Investigación Científica: El estudio de estas reacciones ayuda a los científicos a comprender mejor las interacciones químicas y sus aplicaciones.
Factores que Afectan la Velocidad de las Reacciones
Además del orden de reacción, hay varios factores que pueden influir en la velocidad de las reacciones químicas. Estos factores incluyen la temperatura, la presión, la concentración de los reactivos y la presencia de catalizadores. Cada uno de estos elementos puede tener un impacto significativo en la velocidad de una reacción, independientemente de si es de primer o segundo orden.
La temperatura es un factor clave; en general, al aumentar la temperatura, la velocidad de la reacción también aumenta. Esto se debe a que un aumento en la temperatura proporciona más energía a las moléculas, lo que incrementa la frecuencia y la fuerza de las colisiones entre ellas. Por lo tanto, las reacciones de primer y segundo orden se aceleran a temperaturas más altas, aunque la forma en que se ve afectada puede variar según el orden de la reacción.
La concentración de los reactivos también juega un papel importante. En reacciones de primer orden, un aumento en la concentración de un reactivo aumentará la velocidad de la reacción de manera lineal. Sin embargo, en reacciones de segundo orden, el efecto es más pronunciado, ya que un aumento en la concentración puede llevar a un aumento cuadrático en la velocidad. Por lo tanto, comprender cómo la concentración afecta a cada tipo de reacción es crucial para predecir su comportamiento.
Otros Factores que Influyen en la Velocidad de Reacción
- Presión: En reacciones que involucran gases, un aumento en la presión puede aumentar la velocidad de la reacción al aumentar la concentración de los reactivos gaseosos.
- Catalizadores: La adición de un catalizador puede acelerar una reacción al proporcionar un camino alternativo con una energía de activación más baja.
- Superficie de Contacto: En reacciones heterogéneas, un mayor área de superficie de contacto entre reactivos puede aumentar la velocidad de reacción.
- Estado Físico: El estado físico de los reactivos (sólido, líquido, gas) puede afectar cómo interactúan y, por lo tanto, influir en la velocidad de reacción.
Métodos para Determinar el Orden de Reacción
Para los químicos, determinar el orden de reacción es fundamental para entender cómo se comporta una reacción bajo diferentes condiciones. Existen varios métodos para determinar el orden de reacción, y algunos de los más comunes incluyen el método de la velocidad inicial, el método de integración y el método de medio de vida.
El método de la velocidad inicial implica medir la velocidad de la reacción al inicio, cuando las concentraciones de los reactivos son prácticamente constantes. A partir de estas mediciones, se pueden calcular las órdenes de reacción mediante la comparación de cómo cambia la velocidad al variar las concentraciones de los reactivos.
El método de integración se basa en la integración de las ecuaciones de velocidad. Este método es útil para reacciones de primer y segundo orden, ya que permite obtener relaciones directas entre la concentración y el tiempo, facilitando la obtención de la constante de velocidad y el orden de reacción a partir de datos experimentales.
Otros Métodos para Determinar el Orden de Reacción
- Método de medio de vida: Este método se basa en el tiempo que toma a un reactivo alcanzar la mitad de su concentración inicial. Para reacciones de primer orden, la vida media es constante, mientras que para reacciones de segundo orden, depende de la concentración.
- Método de cambio de concentración: Implica cambiar las concentraciones de los reactivos y observar el efecto en la velocidad de la reacción.
- Análisis de datos cinéticos: El análisis de gráficos de concentración frente al tiempo puede proporcionar información sobre el orden de la reacción observando la forma de la curva resultante.
Conclusiones sobre las Reacciones de Primer y Segundo Orden
Las reacciones de primer y segundo orden representan dos de los tipos más comunes de cinéticas químicas. Comprender las diferencias entre ellas es esencial para la aplicación en la industria, la medicina y la investigación científica. A través de ejemplos prácticos y el estudio de factores que afectan la velocidad de reacción, los químicos pueden predecir y controlar mejor los resultados de las reacciones químicas en diversos contextos.
Las herramientas y métodos disponibles para determinar el orden de reacción permiten a los científicos optimizar procesos y desarrollar nuevas aplicaciones en el campo de la química. En última instancia, el conocimiento sobre reacciones de primer y segundo orden no solo enriquece nuestra comprensión de la química, sino que también tiene un impacto significativo en la vida cotidiana y en el avance de la ciencia.