La ciencia es un campo fascinante que nos ayuda a entender el mundo que nos rodea. Uno de los conceptos fundamentales en la química es la diferencia entre un átomo y un ión. Ambos términos son cruciales para comprender la estructura de la materia y cómo interactúan los elementos químicos. En este artículo, exploraremos en detalle qué son los átomos y los iones, sus características, y cómo se relacionan entre sí. Esta información es esencial para estudiantes y entusiastas de la ciencia que desean profundizar en el tema.
¿Qué es un átomo?
Un átomo es la unidad básica de la materia. Todos los objetos que nos rodean están formados por átomos. Cada átomo está compuesto por tres partículas subatómicas principales: protones, neutrones y electrones. Los protones y los neutrones se encuentran en el núcleo del átomo, mientras que los electrones orbitan alrededor del núcleo. La cantidad de protones en el núcleo determina el elemento químico al que pertenece el átomo. Por ejemplo, un átomo de hidrógeno tiene un protón, mientras que un átomo de oxígeno tiene ocho protones.
La estructura de un átomo es crucial para entender sus propiedades químicas. Los electrones tienen cargas negativas y su disposición en diferentes niveles de energía influye en cómo un átomo interactúa con otros. Esta interacción es lo que da lugar a la formación de moléculas y compuestos. La mayoría de los átomos son eléctricamente neutros porque el número de protones es igual al número de electrones. Sin embargo, esta neutralidad puede cambiar cuando un átomo pierde o gana electrones.
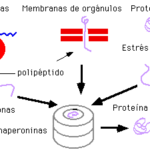 Diferencia entre chaperonas y chaperoninas
Diferencia entre chaperonas y chaperoninas¿Qué es un ion?
Un ión es un átomo o una molécula que ha ganado o perdido uno o más electrones, lo que resulta en una carga eléctrica neta. Si un átomo pierde electrones, se convierte en un ión positivo o catión, ya que tiene más protones que electrones. Por otro lado, si un átomo gana electrones, se convierte en un ión negativo o anión, ya que tiene más electrones que protones. Esta carga eléctrica es fundamental para las reacciones químicas y la formación de compuestos.
Los iones juegan un papel crucial en la química y la biología. Por ejemplo, los iones son esenciales para la conducción de electricidad en soluciones acuosas y son vitales para funciones biológicas, como la transmisión de impulsos nerviosos y la contracción muscular. Además, los iones se forman durante la disolución de sales en agua, donde los compuestos se separan en sus iones constituyentes. Esto permite que los iones interactúen con otras moléculas en el medio.
Diferencias clave entre átomos e iones
Existen varias diferencias clave entre los átomos y los iones. A continuación, se presentan algunos de los aspectos más destacados que los distinguen:
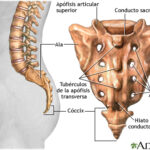 Diferencia entre el sacro y el cóccix
Diferencia entre el sacro y el cóccix- Carga eléctrica: Los átomos son generalmente neutros, mientras que los iones tienen una carga positiva o negativa.
- Composición: Los átomos están compuestos por protones, neutrones y electrones, mientras que los iones son átomos que han perdido o ganado electrones.
- Interacciones químicas: Los iones son más reactivos que los átomos neutros debido a su carga eléctrica, lo que les permite formar enlaces más fácilmente con otros átomos.
Estas diferencias son importantes para comprender cómo se forman los compuestos y cómo interactúan los elementos en diversas reacciones químicas. La carga eléctrica de los iones les permite participar en procesos como la formación de enlaces iónicos, que son fundamentales para la creación de muchos compuestos químicos.
Formación de iones
La formación de iones ocurre a través de un proceso conocido como ionización. Este proceso puede suceder de varias maneras, incluyendo la pérdida o ganancia de electrones. Por ejemplo, cuando un átomo de sodio (Na) pierde un electrón, se convierte en un ion sodio (Na+). Este ion tiene una carga positiva debido a que hay más protones que electrones. De manera similar, cuando un átomo de cloro (Cl) gana un electrón, se convierte en un ion cloruro (Cl–), que tiene una carga negativa.
La ionización puede ocurrir de forma natural, como en el caso de las reacciones químicas, o puede ser inducida por factores externos, como la aplicación de calor o la exposición a la luz. En soluciones acuosas, la ionización es un fenómeno común que permite que las sales se disuelvan y se separen en sus iones constituyentes. Esta propiedad es fundamental para muchas aplicaciones en química y biología.
 Diferencia entre evaporación y ebullición
Diferencia entre evaporación y ebulliciónEjemplos de átomos e iones
Para entender mejor la diferencia entre átomos e iones, es útil considerar algunos ejemplos específicos. Un ejemplo clásico es el sodio y el cloro. El sodio es un átomo que tiene un solo electrón en su capa más externa. Debido a su configuración electrónica, el sodio tiende a perder ese electrón para alcanzar una configuración más estable. Al hacerlo, se convierte en un ion sodio (Na+).
Por otro lado, el cloro tiene siete electrones en su capa más externa y necesita un electrón adicional para completar su nivel de energía. Cuando el cloro gana un electrón, se convierte en un ion cloruro (Cl–). La interacción entre el ion sodio y el ion cloruro da lugar a la formación de cloruro de sodio (NaCl), comúnmente conocido como sal de mesa. Este compuesto es un ejemplo de cómo los átomos y los iones interactúan para formar nuevas sustancias.
Propiedades de los iones
Los iones tienen propiedades únicas que los distinguen de los átomos neutros. Una de las propiedades más importantes es su conductividad eléctrica. Los iones son capaces de conducir electricidad en soluciones acuosas porque pueden moverse libremente y transportar carga eléctrica. Esto es fundamental en procesos como la electrólisis, donde se utilizan iones para conducir electricidad a través de una solución.
Otra propiedad interesante de los iones es su interacción con otros iones y moléculas. Debido a sus cargas opuestas, los iones pueden atraer o repeler a otros iones. Por ejemplo, los iones positivos atraerán a los iones negativos, lo que puede dar lugar a la formación de enlaces iónicos. Esta propiedad es esencial en la química, ya que permite la formación de compuestos y la interacción entre diferentes sustancias.
Importancia de átomos e iones en la vida diaria
Los átomos y los iones son fundamentales en muchos aspectos de nuestra vida diaria. Desde la composición del aire que respiramos hasta los alimentos que consumimos, todo está formado por átomos. Además, los iones desempeñan un papel crucial en procesos biológicos. Por ejemplo, los iones de calcio (Ca2+) son esenciales para la contracción muscular, mientras que los iones de sodio (Na+) y potasio (K+) son vitales para la transmisión de impulsos nerviosos.
En la industria, los átomos y iones son igualmente importantes. Se utilizan en la fabricación de productos químicos, medicamentos y materiales. La comprensión de cómo interactúan los átomos y los iones permite a los científicos desarrollar nuevas tecnologías y mejorar procesos existentes. Por ejemplo, la investigación en baterías y celdas de combustible se basa en la comprensión de la ionización y la movilidad de los iones.
Reacciones químicas y la formación de compuestos
Las reacciones químicas son procesos en los que los átomos e iones se combinan para formar nuevos compuestos. Durante estas reacciones, los enlaces entre los átomos se rompen y se forman nuevos enlaces. Los iones son especialmente importantes en las reacciones de tipo iónico, donde los iones interactúan entre sí para formar compuestos estables. Un ejemplo de esto es la reacción entre el sodio y el cloro para formar cloruro de sodio.
Las reacciones químicas pueden clasificarse en diferentes tipos, como reacciones de combinación, descomposición y desplazamiento. En cada uno de estos tipos de reacciones, los átomos e iones juegan un papel crucial en la transformación de las sustancias. Por ejemplo, en una reacción de desplazamiento, un ion de un compuesto puede ser reemplazado por otro ion, lo que resulta en la formación de un nuevo compuesto.
Conclusión
Entender la diferencia entre átomos e iones es esencial para cualquier persona interesada en la química y la ciencia en general. Los átomos son las unidades básicas de la materia, mientras que los iones son átomos que han ganado o perdido electrones, lo que les confiere una carga eléctrica. Estas diferencias tienen implicaciones significativas en la química, la biología y la vida diaria. La interacción entre átomos e iones es fundamental para comprender cómo se forma la materia y cómo interactúan los diferentes elementos en el mundo que nos rodea.
