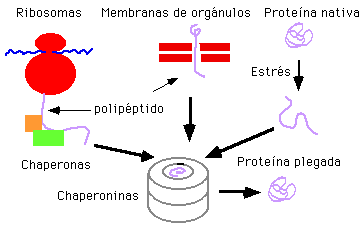
Las chaperonas y chaperoninas son dos tipos de proteínas que desempeñan un papel crucial en la correcta plegadura de otras proteínas dentro de las células. Aunque ambos tipos de proteínas ayudan en el proceso de ensamblaje y mantenimiento de la estructura de las proteínas, existen diferencias significativas en su estructura, función y mecanismo de acción. En este artículo, exploraremos estas diferencias en profundidad, analizando cómo cada tipo de proteína contribuye a la biología celular y su importancia en diversos procesos biológicos.
Definición de chaperonas
Las chaperonas son proteínas que ayudan a otras proteínas a alcanzar su conformación nativa adecuada, evitando que se plieguen de manera incorrecta. Estas proteínas actúan como asistentes durante el proceso de plegado y pueden interactuar con múltiples sustratos. Las chaperonas suelen ser esenciales en situaciones de estrés celular, como el aumento de temperatura o condiciones ambientales adversas, donde las proteínas pueden desnaturalizarse. Además, las chaperonas también pueden participar en el proceso de desplegamiento de proteínas mal plegadas, ayudando a su posterior degradación o refolding.
Una característica notable de las chaperonas es que no forman estructuras complejas como las chaperoninas. En cambio, las chaperonas suelen actuar de manera más flexible y pueden asociarse y disociarse fácilmente de sus sustratos. Este comportamiento les permite adaptarse rápidamente a las necesidades de la célula y responder a cambios en el entorno celular. Las chaperonas son cruciales para mantener la homeostasis celular, asegurando que las proteínas funcionen correctamente en todo momento.
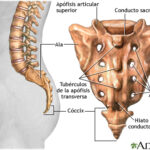 Diferencia entre el sacro y el cóccix
Diferencia entre el sacro y el cóccixDefinición de chaperoninas
Las chaperoninas son un tipo específico de chaperonas que tienen una estructura más compleja y están organizadas en grandes complejos proteicos. Estas proteínas suelen formar estructuras en forma de barril, que proporcionan un entorno aislado donde las proteínas pueden plegarse correctamente. Un ejemplo famoso de chaperonina es el complejo de GroEL/GroES en bacterias, que actúa como un «refugio» para las proteínas en proceso de plegado. La función de las chaperoninas es crucial, ya que su entorno controlado minimiza las interacciones no deseadas que pueden llevar a un plegado incorrecto.
Las chaperoninas requieren un ciclo de ATP para funcionar, lo que significa que utilizan energía para facilitar el plegado de las proteínas. Este ciclo energético es fundamental para su actividad, ya que permite que la chaperonina abra y cierre su estructura, atrapando las proteínas en su interior y promoviendo su correcto plegado. A diferencia de las chaperonas, que pueden interactuar con múltiples sustratos de manera flexible, las chaperoninas suelen tener un sustrato específico y requieren un proceso más estructurado para llevar a cabo su función.
Diferencias estructurales
Una de las principales diferencias entre chaperonas y chaperoninas radica en su estructura. Las chaperonas suelen ser proteínas más pequeñas y menos complejas, mientras que las chaperoninas son grandes complejos proteicos formados por múltiples subunidades. Esta diferencia estructural influye en su modo de acción y en cómo interactúan con otras proteínas. Las chaperonas pueden tener dominios que les permiten unirse a diversas proteínas en diferentes estados de plegado, mientras que las chaperoninas tienen una estructura específica que crea un entorno cerrado y controlado para el plegado de proteínas.
 Diferencia entre evaporación y ebullición
Diferencia entre evaporación y ebulliciónAdemás, las chaperoninas a menudo forman estructuras en forma de barril que pueden contener proteínas en su interior, lo que les permite proporcionar un ambiente seguro para el plegado. Esta estructura es fundamental para su función, ya que evita que las proteínas interactúen con otras moléculas que podrían interferir con el proceso de plegado. En contraste, las chaperonas pueden tener una acción más dispersa y menos específica, interactuando con varias proteínas a la vez y facilitando su plegado en un entorno más abierto.
Mecanismos de acción
El mecanismo de acción de las chaperonas y chaperoninas también varía significativamente. Las chaperonas suelen actuar de manera más directa y rápida, uniendo y liberando proteínas en un proceso que puede ocurrir en segundos. Estas proteínas pueden ayudar a evitar que las proteínas se agreguen o se plieguen incorrectamente, actuando en tiempo real durante el proceso de síntesis proteica. Por ejemplo, durante la traducción de proteínas, las chaperonas pueden unirse a las cadenas polipeptídicas emergentes y ayudar a guiar su plegado.
Por otro lado, las chaperoninas requieren un ciclo más elaborado que involucra el uso de ATP. El proceso comienza con la unión de la proteína sustrato a la chaperonina, seguida de un cambio conformacional que permite el cierre de la estructura en forma de barril. Una vez que la proteína está dentro, la chaperonina proporciona un ambiente cerrado y controlado donde la proteína puede plegarse adecuadamente. Después de un tiempo, la chaperonina utiliza energía del ATP para abrirse nuevamente y liberar la proteína correctamente plegada.
 Diferencia entre Klebsiella oxytoca y Klebsiella pneumoniae
Diferencia entre Klebsiella oxytoca y Klebsiella pneumoniaeFunciones en el estrés celular
Las chaperonas y chaperoninas desempeñan un papel fundamental en la respuesta celular al estrés. En condiciones adversas, como el aumento de temperatura, las proteínas pueden desnaturalizarse o plegarse incorrectamente, lo que puede llevar a la acumulación de proteínas mal plegadas y, en última instancia, a la muerte celular. Las chaperonas ayudan a mitigar estos efectos al unirse a las proteínas desnaturalizadas y guiarlas hacia un plegado correcto o hacia la degradación si no pueden ser reparadas.
Las chaperoninas, por su parte, ofrecen un refugio seguro para las proteínas que están en riesgo de plegarse incorrectamente. Su capacidad para crear un entorno cerrado es especialmente valiosa en situaciones de estrés, ya que minimiza las interacciones no deseadas que podrían resultar en agregados proteicos. En este sentido, tanto las chaperonas como las chaperoninas son esenciales para la supervivencia celular, asegurando que las proteínas mantengan su funcionalidad incluso en condiciones difíciles.
Importancia en enfermedades
Las chaperonas y chaperoninas también están involucradas en diversas enfermedades asociadas con el mal plegado de proteínas. Por ejemplo, en enfermedades neurodegenerativas como el Alzheimer y el Parkinson, las proteínas mal plegadas pueden formar agregados que dañan las células. Las chaperonas juegan un papel protector en estas condiciones, ayudando a prevenir la acumulación de proteínas dañinas. Sin embargo, cuando la carga de proteínas mal plegadas es demasiado alta, las chaperonas pueden verse abrumadas y no pueden cumplir su función adecuadamente.
Las chaperoninas también están implicadas en enfermedades. Su disfunción puede llevar a la acumulación de proteínas mal plegadas, lo que puede contribuir a la progresión de diversas patologías. Por ejemplo, en ciertos tipos de cáncer, la sobreexpresión de chaperoninas ha sido asociada con una mayor resistencia a la terapia, lo que sugiere que estas proteínas pueden ayudar a las células tumorales a sobrevivir en condiciones adversas. Por lo tanto, entender el papel de las chaperonas y chaperoninas en la enfermedad es un área activa de investigación.
Investigación y aplicaciones biotecnológicas
La investigación sobre chaperonas y chaperoninas ha llevado a avances significativos en la biotecnología y la medicina. Por ejemplo, se están explorando métodos para utilizar chaperonas en la producción de proteínas terapéuticas, ya que su capacidad para facilitar el plegado correcto podría mejorar la eficacia y la estabilidad de estas proteínas. Además, se están desarrollando estrategias para diseñar inhibidores de chaperonas y chaperoninas que podrían usarse en el tratamiento de enfermedades como el cáncer, donde la regulación del plegado de proteínas es crucial.
Otro campo de aplicación es la ingeniería de proteínas, donde se utilizan chaperonas y chaperoninas para mejorar la producción de proteínas recombinantes. Estas proteínas son esenciales en la investigación y en la producción de fármacos, por lo que optimizar su plegado y estabilidad puede tener un gran impacto en la industria farmacéutica. La comprensión de los mecanismos de acción de estas proteínas puede abrir nuevas vías para el desarrollo de tratamientos más efectivos y específicos.
Conclusiones sobre chaperonas y chaperoninas
Las chaperonas y chaperoninas son componentes esenciales de la biología celular, desempeñando roles cruciales en el plegado y mantenimiento de las proteínas. A través de sus diferentes estructuras y mecanismos de acción, estas proteínas aseguran que las proteínas se plieguen correctamente y funcionen de manera óptima, lo que es vital para la salud celular y la prevención de enfermedades. La investigación en este campo continúa siendo de gran importancia, con implicaciones en la medicina, la biotecnología y nuestra comprensión general de la biología celular.