En el mundo de la química orgánica, es fundamental entender la estructura y las propiedades de diferentes grupos funcionales. Dos de los grupos funcionales más importantes son el carbonilo y el carboxilo. Aunque pueden sonar similares, tienen características y funciones distintas que son esenciales en la química de los compuestos orgánicos. A continuación, exploraremos en detalle las diferencias entre estos dos grupos funcionales, comenzando por sus definiciones y estructuras básicas.
Definición y Estructura del Carbonilo
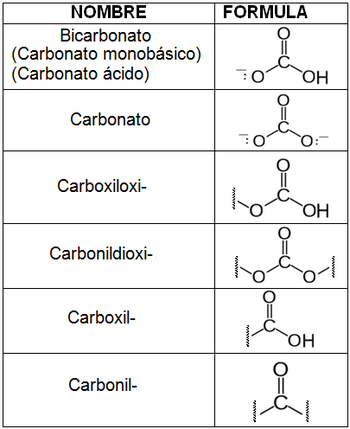
El carbonilo es un grupo funcional que consiste en un átomo de carbono unido a un átomo de oxígeno mediante un doble enlace. Este grupo se encuentra en varios compuestos orgánicos, incluyendo aldehídos y cetonas. La fórmula general del grupo carbonilo es R2C=O, donde R puede ser un hidrógeno o un grupo alquilo. La presencia del doble enlace entre el carbono y el oxígeno es lo que le confiere propiedades químicas únicas. Los carbonilos son muy reactivos y participan en diversas reacciones, como la adición nucleofílica.
La geometría del grupo carbonilo es trigonal plana, lo que significa que los átomos que lo rodean están dispuestos en un plano alrededor del átomo de carbono. Esta disposición se debe a la hibridación sp2 del carbono, lo que permite que los electrones se distribuyan de manera uniforme. Esta estructura es crucial para entender cómo el carbonilo interactúa con otros compuestos en reacciones químicas. La polaridad del enlace C=O también es importante, ya que hace que el carbonilo sea susceptible a ataques nucleofílicos.
 Diferencia entre el ácido folínico y el metilfolato
Diferencia entre el ácido folínico y el metilfolatoDefinición y Estructura del Carboxilo
El carboxilo, por otro lado, es un grupo funcional que combina un grupo carbonilo y un grupo hidroxilo (-OH) en la misma unidad estructural. Su fórmula general es RCOOH, donde R representa un grupo alquilo o un hidrógeno. Este grupo es característico de los ácidos carboxílicos, que son compuestos muy comunes en la química orgánica. La combinación de un grupo carbonilo y un grupo hidroxilo le otorga al carboxilo propiedades ácidas, lo que significa que puede donar un protón (H+) en solución acuosa.
La estructura del carboxilo también es trigonal plana, similar al carbonilo, debido a la hibridación sp2 del carbono. Sin embargo, la presencia del grupo hidroxilo introduce una polaridad adicional que afecta la solubilidad y la reactividad del compuesto. Los ácidos carboxílicos son generalmente más solubles en agua que los aldehídos y cetonas debido a la capacidad del grupo hidroxilo para formar enlaces de hidrógeno con las moléculas de agua. Esto es especialmente relevante en la biología, donde muchos compuestos esenciales son ácidos carboxílicos.
 Diferencia entre genotipificación y secuenciación
Diferencia entre genotipificación y secuenciaciónDiferencias en Reactividad Química
Una de las principales diferencias entre el carbonilo y el carboxilo radica en su reactividad química. Los carbonilos son más susceptibles a reacciones nucleofílicas debido a la polaridad del enlace C=O. Cuando un nucleófilo se acerca a un carbonilo, puede atacar el carbono, lo que lleva a la formación de un intermediario tetraédrico. Este tipo de reacción es fundamental en la síntesis de muchos compuestos orgánicos, incluyendo alcoholes y ácidos carboxílicos.
Por otro lado, el carboxilo, gracias a su naturaleza ácida, puede participar en reacciones de desprotonación. Esto significa que puede perder un protón, formando un ion carboxilato. Esta capacidad de desprotonación es crucial en muchas reacciones biológicas, incluyendo la formación de enlaces peptídicos en proteínas. Además, los ácidos carboxílicos pueden reaccionar con alcoholes en una reacción de esterificación, formando ésteres, que son compuestos muy importantes en la química orgánica y en la fabricación de fragancias y sabores.
Propiedades Físicas
Las propiedades físicas del carbonilo y el carboxilo también muestran diferencias significativas. Los compuestos que contienen el grupo carbonilo, como los aldehídos y cetonas, tienden a tener puntos de ebullición más bajos en comparación con los ácidos carboxílicos. Esto se debe a que los aldehídos y cetonas no pueden formar enlaces de hidrógeno entre moléculas, mientras que los ácidos carboxílicos pueden formar enlaces de hidrógeno intramoleculares e intermoleculares. Esta capacidad de formar enlaces de hidrógeno es lo que les confiere a los ácidos carboxílicos su mayor solubilidad en agua.
 Diferencia entre inmunoprecipitación y Western Blot
Diferencia entre inmunoprecipitación y Western BlotAdemás, los ácidos carboxílicos generalmente tienen un olor más fuerte y característico en comparación con los compuestos carbonilo. Esto se debe a que muchos ácidos carboxílicos son responsables de olores en la naturaleza, como el ácido acético en el vinagre. En cambio, los aldehídos y cetonas suelen tener olores más sutiles. La variación en las propiedades físicas de estos grupos funcionales es fundamental para su identificación y uso en diversas aplicaciones químicas y biológicas.
Ejemplos Comunes de Carbonilos y Carboxilos
En la química orgánica, hay muchos ejemplos comunes de compuestos que contienen grupos carbonilo y carboxilo. Algunos de los aldehídos más conocidos incluyen el formaldehído y el benzaldehído. El formaldehído es un compuesto simple que se utiliza en la fabricación de resinas y en la preservación de tejidos biológicos. Por otro lado, el benzaldehído es conocido por su aroma a almendra y se utiliza en la producción de sabores y fragancias.
En el caso de los ácidos carboxílicos, el ácido acético es uno de los ejemplos más reconocidos. Es el componente principal del vinagre y se utiliza ampliamente en la industria alimentaria y química. Otro ejemplo es el ácido benzoico, que se utiliza como conservante en alimentos y en la fabricación de productos farmacéuticos. La diversidad de compuestos que contienen estos grupos funcionales resalta su importancia en la química y en aplicaciones prácticas.
Aplicaciones en la Industria
Los grupos funcionales carbonilo y carboxilo tienen diversas aplicaciones en la industria. Por ejemplo, los compuestos carbonilo se utilizan en la fabricación de plásticos, resinas y productos químicos intermedios. Las cetonas, como la acetona, son solventes comunes en la industria de pinturas y lacas. Además, los aldehídos se utilizan en la síntesis de productos farmacéuticos y agroquímicos, lo que demuestra su relevancia en la producción industrial.
En cuanto a los ácidos carboxílicos, su capacidad para actuar como ácidos les permite ser utilizados en la fabricación de productos químicos, como detergentes y surfactantes. El ácido acético, por ejemplo, se utiliza en la producción de acetato de polivinilo, un material ampliamente utilizado en adhesivos y revestimientos. Además, los ácidos carboxílicos son esenciales en la producción de biocombustibles y en la industria alimentaria, donde actúan como conservantes y saborizantes.
Diferencias en la Solubilidad
La solubilidad es otro aspecto donde se observan diferencias marcadas entre los compuestos que contienen grupos carbonilo y carboxilo. Como se mencionó anteriormente, los ácidos carboxílicos son generalmente más solubles en agua que los aldehídos y cetonas. Esta mayor solubilidad se debe a la capacidad de los ácidos carboxílicos para formar enlaces de hidrógeno con el agua. La polaridad del grupo hidroxilo (-OH) en el carboxilo es crucial para esta interacción, mientras que los carbonilos, al carecer de un grupo hidroxilo, no pueden formar enlaces de hidrógeno de la misma manera.
Los compuestos carbonilo, como las cetonas y aldehídos, tienden a ser menos solubles en agua a medida que aumenta el tamaño de la cadena carbonada. Esto se debe a que la parte no polar de la molécula se vuelve más dominante, lo que reduce la capacidad de interacción con el agua. Sin embargo, los ácidos carboxílicos, incluso aquellos con cadenas más largas, pueden seguir siendo solubles en agua debido a la presencia del grupo carboxilo, que es altamente polar. Esta diferencia en solubilidad es crucial en aplicaciones biológicas y químicas, donde la solubilidad en agua puede influir en la biodisponibilidad y la reactividad de los compuestos.
Reacciones Comunes de Carbonilos y Carboxilos
Ambos grupos funcionales participan en una variedad de reacciones químicas que son esenciales en la síntesis orgánica. Por ejemplo, los carbonilos pueden sufrir reacciones de adición nucleofílica, donde un nucleófilo ataca el carbono carbonílico. Esta reacción es fundamental en la formación de alcoholes a partir de aldehídos y cetonas. Además, los carbonilos pueden ser oxidados a ácidos carboxílicos, lo que ilustra su papel en reacciones redox.
Por su parte, los ácidos carboxílicos son conocidos por participar en reacciones de esterificación, donde reaccionan con alcoholes para formar ésteres y agua. Esta reacción es de gran importancia en la industria de fragancias y sabores, así como en la producción de polímeros. Además, los ácidos carboxílicos pueden sufrir reacciones de deshidratación para formar anhidridios, lo que demuestra su versatilidad en la química orgánica. La comprensión de estas reacciones es fundamental para los químicos que buscan sintetizar nuevos compuestos y materiales.
Conclusión sobre la Importancia de la Comprensión de Carbonilos y Carboxilos
Entender las diferencias entre los grupos funcionales carbonilo y carboxilo es esencial para cualquier persona interesada en la química orgánica. Estos grupos no solo tienen estructuras y propiedades diferentes, sino que también juegan roles cruciales en una variedad de reacciones químicas y aplicaciones industriales. Desde la producción de compuestos farmacéuticos hasta la creación de nuevos materiales, la química de carbonilos y carboxilos es fundamental en la ciencia moderna.