El estudio de las propiedades electroquímicas de las superficies es fundamental en diversas áreas de la ciencia, especialmente en la química y la biología. Entre los conceptos clave en este ámbito se encuentran el potencial zeta y el potencial de Nernst. Ambos son parámetros que describen comportamientos eléctricos en sistemas de partículas cargadas, pero tienen orígenes y aplicaciones distintas. En este artículo, exploraremos en detalle cada uno de estos conceptos, sus diferencias, y cómo se aplican en diferentes contextos científicos.
¿Qué es el potencial zeta?
El potencial zeta es una medida de la carga eléctrica en la interfaz entre una partícula y un líquido. Esta carga se genera debido a la disociación de iones en la superficie de la partícula, lo que crea una doble capa eléctrica. Esta doble capa está compuesta por una capa de iones fijos y una capa de iones móviles que se distribuyen en el líquido. La medida del potencial zeta se realiza generalmente utilizando técnicas de electroforesis o microelectrodos.
El potencial zeta es crucial en procesos como la estabilización de coloides, donde las partículas suspendidas deben mantenerse separadas para evitar la coagulación. Cuando el potencial zeta es alto, las partículas repelen entre sí, lo que favorece la estabilidad de la suspensión. Por otro lado, un potencial zeta bajo puede llevar a la agregación de partículas, lo que es indeseable en muchas aplicaciones industriales y biológicas.
 Diferencia entre estromatolitos y trombolitos
Diferencia entre estromatolitos y trombolitosFactores que afectan el potencial zeta
- pH del medio: Cambios en el pH pueden alterar la carga superficial de las partículas.
- Concentración iónica: Un aumento en la concentración de iones en la solución puede disminuir el potencial zeta.
- Tipo de ion: Diferentes iones tienen diferentes efectos en la carga de la superficie.
Estos factores son cruciales para entender cómo se comportan las partículas en diferentes condiciones. Por ejemplo, en un medio ácido, muchas partículas pueden adquirir una carga positiva, lo que afectará su interacción con otras partículas o superficies. En contraste, en un medio básico, pueden volverse negativas. Esta variabilidad en el potencial zeta es un aspecto esencial para el diseño de sistemas en química, biología y materiales.
¿Qué es el potencial de Nernst?
El potencial de Nernst, por otro lado, se refiere al potencial eléctrico que se desarrolla a través de una membrana semipermeable cuando hay una diferencia de concentración de iones a ambos lados de la membrana. Este concepto es fundamental en la electroquímica y es especialmente relevante en el estudio de las células electroquímicas y los procesos biológicos, como la transmisión de impulsos nerviosos.
La ecuación de Nernst permite calcular el potencial de equilibrio para un ion específico, considerando las concentraciones del ion en ambos lados de la membrana. Esto es importante porque determina cómo se moverán los iones a través de la membrana, influyendo en procesos como la osmósis y la difusión. Por ejemplo, en el caso de las neuronas, el potencial de Nernst es clave para entender cómo se generan y propagan los impulsos eléctricos.
 Diferencia entre isótopos e isobaras
Diferencia entre isótopos e isobarasLa ecuación de Nernst
La ecuación de Nernst se expresa generalmente de la siguiente manera:
E = E0 + (RT/nF) ln([ionin]/[ionout])
Donde:
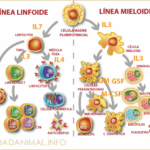 Diferencia entre células mieloides y linfoides
Diferencia entre células mieloides y linfoides- E: Potencial de Nernst.
- E0: Potencial estándar.
- R: Constante de los gases.
- T: Temperatura en Kelvin.
- n: Número de electrones transferidos.
- F: Constante de Faraday.
Esta ecuación muestra cómo el potencial eléctrico está directamente relacionado con la concentración de iones, lo que es esencial para comprender cómo las células mantienen su equilibrio iónico y su potencial de membrana. Por lo tanto, el potencial de Nernst es una herramienta fundamental en la biología celular y la neurociencia.
Diferencias clave entre el potencial zeta y el potencial de Nernst
A pesar de que tanto el potencial zeta como el potencial de Nernst son conceptos relacionados con la carga eléctrica y la interacción de iones, hay diferencias significativas entre ellos. La primera diferencia radica en su definición y contexto de aplicación. Mientras que el potencial zeta se refiere a la carga en la superficie de partículas en suspensión, el potencial de Nernst se centra en el equilibrio de iones a través de membranas. Esta diferencia fundamental en su enfoque los hace aplicables en contextos muy distintos.
Otra diferencia importante es la forma en que se mide cada uno. El potencial zeta se mide generalmente a través de técnicas experimentales como la microelectroforesis, mientras que el potencial de Nernst se calcula a partir de concentraciones de iones utilizando la ecuación de Nernst. Esto implica que el potencial zeta es una propiedad más relacionada con la física de las partículas, mientras que el potencial de Nernst se relaciona más con procesos químicos y biológicos.
Aplicaciones prácticas
- Potencial Zeta: Utilizado en la industria de alimentos, farmacéutica y cosmética para asegurar la estabilidad de emulsiones y suspensiones.
- Potencial de Nernst: Fundamental en el desarrollo de baterías, celdas de combustible y en el estudio de la fisiología celular.
Las aplicaciones del potencial zeta son particularmente relevantes en la industria de alimentos y productos farmacéuticos, donde la estabilidad de coloides y emulsiones es crucial. Por otro lado, el potencial de Nernst es esencial en el diseño de sistemas electroquímicos, como baterías y celdas de combustible, así como en la investigación biomédica, donde se estudia el funcionamiento de las células y su respuesta a diferentes condiciones ambientales.
Importancia en la investigación científica
Ambos conceptos son fundamentales en la investigación científica actual. El potencial zeta es clave para entender la estabilidad de sistemas coloidales, lo que es vital en la formulación de productos. En investigaciones sobre nanopartículas y materiales avanzados, el potencial zeta puede influir en la interacción entre partículas y su funcionalidad. Esto es especialmente importante en campos como la medicina, donde las nanopartículas se utilizan para la entrega de fármacos.
Por otro lado, el potencial de Nernst es fundamental para comprender la bioelectricidad. En la neurociencia, por ejemplo, el estudio del potencial de Nernst de diferentes iones es crucial para entender cómo las neuronas generan impulsos eléctricos y cómo se comunican entre sí. Esto tiene implicaciones no solo en la biología, sino también en la medicina, ya que muchas enfermedades están relacionadas con disfunciones en la transmisión de señales eléctricas en el sistema nervioso.
Interacciones entre ambos potenciales
Aunque el potencial zeta y el potencial de Nernst se utilizan en contextos diferentes, también pueden interactuar en ciertos sistemas. Por ejemplo, en soluciones donde hay partículas cargadas que pueden afectar la distribución de iones, el potencial zeta puede influir en la forma en que se establece un potencial de Nernst. Esto es especialmente relevante en sistemas biológicos, donde la interacción entre células y su entorno puede modificar tanto el potencial zeta como el potencial de Nernst, afectando la función celular.
Además, en aplicaciones tecnológicas, como el desarrollo de sensores electroquímicos, tanto el potencial zeta como el potencial de Nernst pueden ser considerados para optimizar el rendimiento de dispositivos que dependen de la interacción entre iones y superficies. Por lo tanto, aunque son conceptos distintos, la comprensión de ambos es crucial para la investigación y el desarrollo en múltiples disciplinas científicas.
Conclusiones sobre el potencial zeta y el potencial de Nernst
el potencial zeta y el potencial de Nernst son dos conceptos electroquímicos que, aunque están relacionados con la carga y el movimiento de iones, se aplican en contextos diferentes y tienen diferentes métodos de medición. El potencial zeta se centra en la estabilidad de las partículas en suspensión, mientras que el potencial de Nernst se ocupa de las diferencias de concentración de iones a través de membranas. Ambos son esenciales para comprender fenómenos en química, biología y tecnología, y su estudio sigue siendo un área activa de investigación en la ciencia moderna.
